题目内容
4.用分子、原子、离子填空:(1)构成物质的微粒分子、原子和离子(2)不带电的微粒是分子、原子
(3)参加化学反应时,一定发生变化的是分子,一定没有发生变化的是原子.
分析 (1)根据物质的构成微粒解答;
(2)根据已有的微粒带电性的知识进行解答即可;
(3)根据化学反应的实质解答.
解答 解:(1)构成物质的基本微粒是分子、原子和离子;
(2)分子、原子是呈电中性的微粒;
(3)参加化学反应时,一定发生变化的是分子,一定没有发生变化的是原子.
答案:(1)分子、原子和离子;
(2)分子、原子;
(3)分子;原子.
点评 本题考查了有关物质的微粒构成以及电性的知识,要求同学们加强对基础知识的储备,以便灵活应用.

练习册系列答案
相关题目
14.下列变化属于化学变化的是( )
| A. | 烧开水 | B. | 电解水 | C. | 水结冰 | D. | 蔗糖溶于水 |
12.某工化肥厂需大量二氧化碳生产化肥,欲购进一批石灰石(其中杂质不参加任何反应),厂家到产地取样分析以确定价格.他们取样2克,并把20克稀盐酸分四次加入,充分反应后,每次剩余固体质量见表
试计算:
(1)2克石灰石样品中含有杂质的质量是0.4克.
(2)石灰石样品中碳酸钙的质量分数是多少?
(3)1000千克这种石灰石充分煅烧后,可得二氧化碳质量是多少?( CaCO3$\frac{\underline{\;高温\;}}{\;}$ CaO+CO2↑ )
| 稀盐酸的用量 | 剩余固体的质量/g |
| 第一次加入5g | 1.4g |
| 第二次再加入5g | 0.8g |
| 第三次再加入5g | 0.4g |
| 第四次再加入5g | 0.4g |
(1)2克石灰石样品中含有杂质的质量是0.4克.
(2)石灰石样品中碳酸钙的质量分数是多少?
(3)1000千克这种石灰石充分煅烧后,可得二氧化碳质量是多少?( CaCO3$\frac{\underline{\;高温\;}}{\;}$ CaO+CO2↑ )
19.根据化学方程式Na2CO3+2A═H2O+2B+CO2↑,推断B、A的相对分子质量差为( )
| A. | 44 | B. | 33 | C. | 22 | D. | 11 |
14.下列物质敞口放置在空气中较长时间,无明显变化的是( )
| A. | 浓盐酸 | B. | 生石灰 | C. | 氯化钠溶液 | D. | 浓硫酸 |
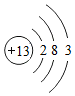 (1)用正确的化学用语填空:
(1)用正确的化学用语填空: 表示的微粒是Cl.
表示的微粒是Cl.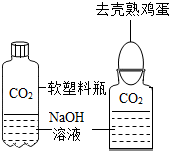 该兴趣小组同学将制得的CO2分别通人澄清石灰水和氢氧化钠溶液中,他们观察到前者变浑浊,后者无明显现象.CO2和NaOH是否发生了化学反应?
该兴趣小组同学将制得的CO2分别通人澄清石灰水和氢氧化钠溶液中,他们观察到前者变浑浊,后者无明显现象.CO2和NaOH是否发生了化学反应?