题目内容
3.将8克不纯的锌片(杂质与酸不反应)投入到一个装有150克稀硫酸烧杯中,恰好完全反应,生成了0.2克氢气.(1)求不纯锌片的纯度?
(2)求该稀硫酸溶液的溶质质量分数?
分析 (1)根据化学方程式得出各物质之间的质量比,列出比例式,依据氢气的质量通过计算得出生成锌的质量,然后求出其质量分数即可;
(2)根据氢气的质量可以计算出硫酸的质量,然后求出溶质的质量分数即可.
解答 解:(1)设锌的质量为x,H2SO4的质量为y
Zn+H2SO4═ZnSO4+H2↑
65 98 2
x y 0.2g
$\frac{65}{x}$=$\frac{98}{y}$=$\frac{2}{0.2g}$
解得:x=6.5g y=9.8g
所以锌的纯度为:$\frac{6.5g}{8g}$×100%=81.25%
(2)稀硫酸溶液的溶质质量分数为:$\frac{9.8g}{150g}$×100%=6.5%
答:(1)不纯锌片的纯度为81.25%;
(2)该稀硫酸溶液的溶质质量分数为6.5%.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
相关题目
8.盐在日常生活中是用途非常广泛的一类物质,下列说法中不正确的是( )
| A. | 添加大量的亚硝酸钠来保鲜食品 | B. | 道路积雪可撒食盐以促进冰雪融化 | ||
| C. | 农业上常用硫酸铜配制波尔多液 | D. | 用纯碱除去面粉发酵生成的酸 |
1.下列有关资源的叙述不正确的是( )
| A. | 天然气是最清洁的燃料 | |
| B. | 稀土有“工业的维生素”的美誉,是不可再生的重要战略资源 | |
| C. | 地球表面约71%被水覆盖 | |
| D. | 空气的成分按体积计大约是:氧气21%、氮气78%、稀有气体等其它成分l% |
5.某研究小组欲检验草酸晶体样品分解产物,并测定样品中草酸晶体的质量分数(假设杂质不参与反应).已知:浓硫酸可作为干燥剂;草酸晶体(H2C2O4•2H2O )的性质见表:
(1)图1是加热装置.

最适宜的加热分解草酸晶体装置是c(填图1装置序号a、b、c).不选另外两装置的原因是(说明不选的装置的序号和对应的理由):①a,固体药品熔化后会流到试管口.②b,冷凝水会倒流到试管底,造成试管破裂.
(2)图2是验证热分解产物中含CO、CO2的装置.
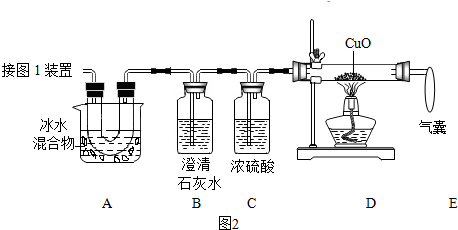
①装置A的作用是除去草酸蒸气,防止对二氧化碳的检验产生干扰,气囊的作用是收集未反应的一氧化碳,防止空气污染.
②证明存在CO2的现象是澄清石灰水变浑浊.证明存在CO的现象是D中黑色固体变红.
(3)为测定样品中草酸晶体的质量分数,设计如下方案:称取一定量样品,用上述装置进行实验,称量装置D反应前后的质量差.由此计算出的实验结果比实际值偏低,排除仪器和操作因素,其可能原因:一氧化碳没有全部与氧化铜反应.
| 熔点 | 沸点 | 热稳定性 | 其他 |
| 101℃~102℃ | 150℃~160℃升华 | 100.1℃分解出水,175℃分解成CO2、CO、H2O | 与 Ca(OH)2反应产生白色沉淀(CaC2O4) |

最适宜的加热分解草酸晶体装置是c(填图1装置序号a、b、c).不选另外两装置的原因是(说明不选的装置的序号和对应的理由):①a,固体药品熔化后会流到试管口.②b,冷凝水会倒流到试管底,造成试管破裂.
(2)图2是验证热分解产物中含CO、CO2的装置.

①装置A的作用是除去草酸蒸气,防止对二氧化碳的检验产生干扰,气囊的作用是收集未反应的一氧化碳,防止空气污染.
②证明存在CO2的现象是澄清石灰水变浑浊.证明存在CO的现象是D中黑色固体变红.
(3)为测定样品中草酸晶体的质量分数,设计如下方案:称取一定量样品,用上述装置进行实验,称量装置D反应前后的质量差.由此计算出的实验结果比实际值偏低,排除仪器和操作因素,其可能原因:一氧化碳没有全部与氧化铜反应.
8.臭氧(O3)能吸收大部分紫外线,保护地球生物.它属于( )
| A. | 纯净物 | B. | 混合物 | C. | 氧气的一种 | D. | 化合物 |
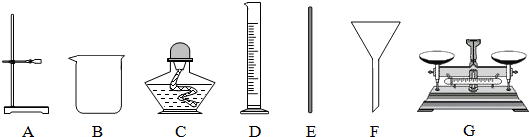
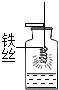 规范的操作是实验安全和成功的保证.按如图所示做细铁丝在氧气中燃烧的实验时,若事先未在瓶底铺一层细沙或装入少量的水,可能出现的后果是生成物熔化溅落下来炸裂集气瓶;铁丝在氧气中燃烧的化学方程式为3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;若实验中铁丝未燃烧,造成实验失败的原因可能是铁丝上的锈没有除净;氧气的纯度不高;铁丝没有预热(合理均可).
规范的操作是实验安全和成功的保证.按如图所示做细铁丝在氧气中燃烧的实验时,若事先未在瓶底铺一层细沙或装入少量的水,可能出现的后果是生成物熔化溅落下来炸裂集气瓶;铁丝在氧气中燃烧的化学方程式为3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;若实验中铁丝未燃烧,造成实验失败的原因可能是铁丝上的锈没有除净;氧气的纯度不高;铁丝没有预热(合理均可).