题目内容
18.一定质量的氢氧化钠和63g溶质质量分数为20%的硝酸溶液恰好完全反应.计算:(1)需氢氧化钠多少克?
(2)反应后所形成的溶液中溶质质量分数是多少?
分析 根据稀硝酸的质量、溶质质量分数可以计算HNO3的质量,根据HNO3的质量可以计算氢氧化钠的质量和反应生成硝酸钠的质量,进一步可以计算反应后溶液中溶质的质量分数.
解答 解:(1)设需要氢氧化钠的质量为x,生成硝酸钠的质量为x,
NaOH+HNO3═NaNO3+H2O
40 63 85
x 63g×20% y
$\frac{40}{x}=\frac{63}{63g×20%}=\frac{85}{y}$
x=8g
y=17g
(2)反应后所形成的溶液中溶质质量分数=$\frac{17g}{8g+63g}×100%$=23.9%
答:(1)需氢氧化钠为8g;
(2)反应后所形成的溶液中溶质质量分数为23.9%.
点评 本题主要考查学生运用化学方程式进行计算和推断的能力,比较简单,计算时要注意规范性和准确性.

练习册系列答案
相关题目
9.下列问题的研究中,未利用对比实验思想方法的是( )
| A. | 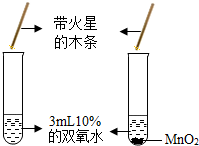 | B. | 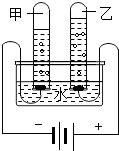 | ||
| C. | 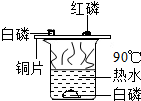 | D. |  |
13.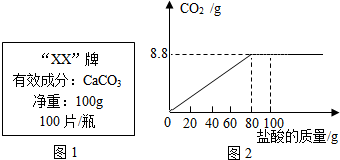 钙是人体中的常量元素,缺钙时可通过使用保健药剂来增加摄入量,某补钙药剂说明书的部分信息如图所示.现将100g盐酸分成5等份,逐次加到用40片该药剂制成的粉末中(其他成分不参与盐酸反应),得到部分数据与图象如下.请根据有关信息回答问题.
钙是人体中的常量元素,缺钙时可通过使用保健药剂来增加摄入量,某补钙药剂说明书的部分信息如图所示.现将100g盐酸分成5等份,逐次加到用40片该药剂制成的粉末中(其他成分不参与盐酸反应),得到部分数据与图象如下.请根据有关信息回答问题.
(1)该品牌补钙药剂中CaCO3的质量分数是50%,a的数值为25.
(2)求该盐酸中溶质的质量分数(写出计算过程,计算结果保留一位小数).
 钙是人体中的常量元素,缺钙时可通过使用保健药剂来增加摄入量,某补钙药剂说明书的部分信息如图所示.现将100g盐酸分成5等份,逐次加到用40片该药剂制成的粉末中(其他成分不参与盐酸反应),得到部分数据与图象如下.请根据有关信息回答问题.
钙是人体中的常量元素,缺钙时可通过使用保健药剂来增加摄入量,某补钙药剂说明书的部分信息如图所示.现将100g盐酸分成5等份,逐次加到用40片该药剂制成的粉末中(其他成分不参与盐酸反应),得到部分数据与图象如下.请根据有关信息回答问题. | 第1次 | 第3次 | 第4次 | 第5次 | |
| 加入盐酸的质量(g) | 20 | 20 | 20 | 20 |
| 剩余固体的质量(g) | 35 | a | 20 | 20 |
(2)求该盐酸中溶质的质量分数(写出计算过程,计算结果保留一位小数).
20.下列化学方程式书写正确的是( )
| A. | 2P+5O2$\frac{\underline{\;点燃\;}}{\;}$P2O5 | B. | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | ||
| C. | 2CO+O2═2CO2 | D. | H2O$\frac{\underline{\;通电\;}}{\;}$H2+02 |
1.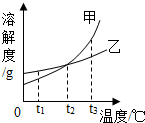 甲、乙两固体物质的溶解度曲线如图所示.下列说法不正确的是( )
甲、乙两固体物质的溶解度曲线如图所示.下列说法不正确的是( )
 甲、乙两固体物质的溶解度曲线如图所示.下列说法不正确的是( )
甲、乙两固体物质的溶解度曲线如图所示.下列说法不正确的是( )| A. | t1℃时,甲物质的溶解度小于乙物质的溶解度 | |
| B. | t2℃时,甲、乙两物质的饱和溶液中分别含甲、乙两物质的质量相等 | |
| C. | 将t3℃的甲、乙两物质的饱和溶液降温至t1℃时,都会析出晶体 | |
| D. | 甲、乙两物质的溶解度均随温度的升高而增大 |