题目内容
2.下列反应中,属于分解反应,且生成物都是氧化物的是( )| A. | 电解水 | B. | 加热高锰酸钾固体 | ||
| C. | 煅烧石灰石 | D. | 加热碳酸 |
分析 分解反应:一种物质反应后生成两种或两种以上的物质,其特点可总结为“一变多”;氧化物是只含有两种元素且其中一种元素是氧元素的化合物,据此进行分析判断.
解答 解:A、电解水生成氢气和氧气,该反应符合“一变多”的特征,属于分解反应;但生成物氢气和氧气均属于单质,故选项错误.
B、加热高锰酸钾固体生成锰酸钾、二氧化锰和氧气,该反应符合“一变多”的特征,属于分解反应;但生成物中氧气是单质,锰酸钾由三种元素组成,不属于氧化物;故选项错误.
C、煅烧石灰石生成氧化钙和二氧化碳,该反应符合“一变多”的特征,属于分解反应;且氧化钙、二氧化碳均是由2种元素组成的,且一种元素是氧元素,均属于氧化物;故选项正确.
D、碳酸分解生成水和二氧化碳,该反应符合“一变多”的特征,属于分解反应;且水、二氧化碳均是由2种元素组成的,且一种元素是氧元素,均属于氧化物;故选项正确.
故选:CD.
点评 本题难度不大,掌握分解反应的特征(“一变多”)、氧化物的特征是正确解答本题的关键.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
3.2015年“6.5”世界环境日中国主题是“低碳减排•绿色生活”,下列说法与该主题不相符的是( )
| A. | 白天光线充足时将教室的灯关闭 | B. | 草稿纸双面使用 | ||
| C. | 多开私家车少走路节约时间 | D. | 用传统发条式闹钟代替电子钟 |
4.氢化钙固体时登山运动员常用的能源提供剂,某探究小组的同学通过查阅资料得知,氢化钙(CaH2)和水反应生成氢氧化钙和氢气,请用化学方程式表示其反应CaH2+2H2O═Ca(OH)2+2H2↑.
探究小组的同学把一定量的CaH2加入Na2CO3溶液中,充分反应后过滤,得到滤渣和滤液.经检验滤渣的成分是碳酸钙.
【提出问题】滤液中溶质的成分是什么?
【猜想与假设】
猜想一:NaOH 猜想二:NaOH、Ca(OH)2
猜想三:NaOH、Na2CO3 猜想四:NaOH、Na2CO3、Ca(OH)2
经过讨论,大家一致认为猜想四不合理,请用化学方程式说明原因Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
【实验验证】
【反思与拓展】①若向NH4Cl的溶液中加一定量CaH2,充分反应,产生的气体是氢气和氨气.
②登山运动员常用CaH2作为能源提供剂,与氢气相比,其优点是携带和使用比氢气安全、方便.
探究小组的同学把一定量的CaH2加入Na2CO3溶液中,充分反应后过滤,得到滤渣和滤液.经检验滤渣的成分是碳酸钙.
【提出问题】滤液中溶质的成分是什么?
【猜想与假设】
猜想一:NaOH 猜想二:NaOH、Ca(OH)2
猜想三:NaOH、Na2CO3 猜想四:NaOH、Na2CO3、Ca(OH)2
经过讨论,大家一致认为猜想四不合理,请用化学方程式说明原因Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
【实验验证】
| 实验 | 现象 | 结论 |
| 实验一:取滤液,向其中滴入少量碳酸钠溶液 | 无明显现象 | 猜想 二 不成立 |
| 实验二:另取滤液,向其中加入足量稀盐酸 | 先无变化后产生气泡 | 猜想三成立 |
②登山运动员常用CaH2作为能源提供剂,与氢气相比,其优点是携带和使用比氢气安全、方便.
1.化学与生产、生活密切不可分,身边处处有化学,下列说法不正确的是( )
| A. | 用烧碱改良酸性土壤,处理酸性污水 | |
| B. | 食品包装袋内充氮气延长食品保质期 | |
| C. | 察觉燃气泄漏要关闭阀门,开窗通风 | |
| D. | 用煮沸的方法降低水的硬度 |
11.设计实验方案是科学探究的重要环节,以下化学实验设计中,不能达到实验目的是( )
| A. | 厨房中用食醋鉴别纯碱与食盐 | |
| B. | 用AgNO3溶液验证H2中混有的少量HCl杂质 | |
| C. | 用稀硫酸除去铁粉中混有的少量铜粉 | |
| D. | 用稀盐酸检验暴露在空气中的NaOH固体是否变质 |
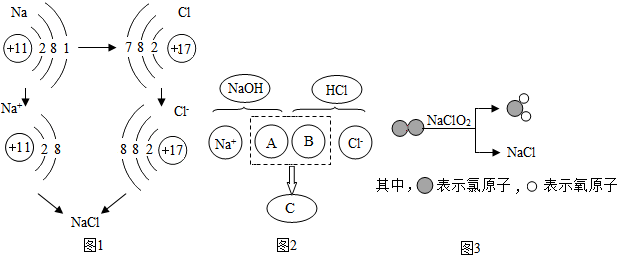
 ,该原子的质子数为12,它在化学反应中容易失去(填“得到”或“失去”)电子.
,该原子的质子数为12,它在化学反应中容易失去(填“得到”或“失去”)电子.