题目内容
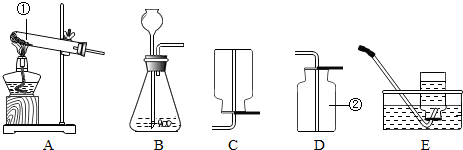
8.乙炔(C2H2)气体和氧气反应能产生高温火焰,工人师傅常用氧炔焰切割或焊接金属.乙炔由碳化钙(块状固体,化学式为CaC2)与水反应生成,同时生成一种白色固体.(1)已知碳化钙与水反应非常剧烈,乙炔的密度比空气略小.实验室欲制取并收集纯净的乙炔,要求做到节约、安全,你选择的装置是CF(选填图中装置序号).

(2)写出乙炔在空气中燃烧的化学方程式:2C2H2+5O2$\frac{\underline{\;点燃\;}}{\;}$4CO2+2H2O.
分析 (1)根据反应物的状态和反应条件确定发生装置,收集纯净的气体通常用排水法,并结合仪器的用途分析解答;
(2)据反应原理书写方程式.
解答 解:(1)乙炔由碳化钙(块状固体,化学式为CaC2)与水常温下反应生成,但反应非常剧烈,故发生装置可选C,因分液漏斗可通过控制水的量,控制反应速率,安全,并能通过旋转活栓控制反应随时发生、随时停止,当收集完气体后,可不再滴加液体达到节约的目的,而长颈漏斗则不可以;收集装置是F,因为乙炔难溶于水,排水法收集的气体比较纯净;故实验室欲制取并收集纯净的乙炔,要求做到节约、安全,可选择的装置是CF;
(2)乙炔在空气中点燃生成二氧化碳和水,反应的化学方程式是:2C2H2+5O2$\frac{\underline{\;点燃\;}}{\;}$4CO2+2H2O;
故答案为:
(1)CF;
(2)2C2H2+5O2$\frac{\underline{\;点燃\;}}{\;}$4CO2+2H2O.
点评 明确发生和收集装置的选取方法,收集纯净气体用排水法,并能据反应原理正确书写方程式是解答此题的关键.

练习册系列答案
相关题目
18.下列说法中,正确的是( )
| A. | 有多种反应物的反应一定是化合反应 | |
| B. | 氧化反应一定是化合反应 | |
| C. | 有氧气参加的反应一定是氧化反应 | |
| D. | 化合反应一定是氧化反应 |
16.有Na、S、O、H四种元素中的二种或三种元素组成四种常见的化合物.其中甲能跟盐酸反应生成盐和水;乙能跟氯化钡反应生成一种硫酸盐和另一种盐;丙能跟氢氧化钠反应生成盐和水;丁呈中性,且可以分别跟氧化钙或二氧化碳发生化合反应,生成相应的碱或酸.下列推断:①甲一定是氢氧化钠;②乙一定是硫酸钠;③丙可能是硫酸;④丁一定是水.其中正确的一组是( )
| A. | ①②③ | B. | ①②④ | C. | ①③④ | D. | ②③④ |
3.除去下列物质中所含杂质的方法正确的是( )
| 物 质 | 杂 质 | 除杂试剂 | 提 纯 方 法 | |
| A | CO2 | CO | O2 | 点燃 |
| B | KCl | MnO2 | 水 | 充分溶解、过滤、蒸发 |
| C | NaCl | Na2CO3 | 硝酸 | 足量加入硝酸溶液 |
| D | Cu(NO3)2溶液 | AgNO3 | 铁粉 | 加入少量的铁粉,过滤 |
| A. | A | B. | B | C. | C | D. | D |
20.除去下列各物质中混有的少量杂质,所用试剂正确的是( )
| 序号 | 物质 | 杂质 | 所用试剂 |
| A | 氧气 | 氯化氢 | 氢氧化钠溶液 |
| B | 二氧化硫 | 水 | 碱石灰 |
| C | 氧化钙 | 碳酸钙 | 适量的稀盐酸 |
| D | 氢氧化钠 | 碳酸钠 | 适量的氯化钡溶液 |
| A. | A | B. | B | C. | C | D. | D |