题目内容
实验室用溶质质量分数为10%氢氧化钠溶液进行水的电解实验.
实验一:配制100g溶质质量分数为10%氢氧化钠溶液.
(1)所需的氢氧化钠质量: g;
(2)称量时,氢氧化钠固体应放于天平 (填“左”或“右”)盘的烧杯内;量取的需的水(水的密度为1g/cm3),应选择的量筒的规格是 mL(选填“10”、“100”或“250”).
实验二:水的电解实验
用如图装置进行水的电解实验.已知氢氧化钠在水的电解实验中,只起到增强水的导电性作用.
(3)开始反应前a,b两管内都充满溶液.关闭活塞,接通电源,一段时间后,两管产生的气体如图所示,则a管下方导线应接电源的 极(填“正”或“负”).用 验证b管中的气体,写出电解水的化学方程式: .
(4)说明水是一种化合物的实验事实: .
(5)电解后溶液的溶质质量分数 10%(填“<”、“=”或“>”).

| 一定溶质质量分数的溶液的配制;测量容器-量筒;称量器-托盘天平;常见气体的检验与除杂方法;电解水实验;书写化学方程式、文字表达式、电离方程式.菁优网版权所有 | |
| 专题: | 溶液、浊液与溶解度;空气与水. |
| 分析: | 根据已有的知识进行分析,溶质质量=溶液质量×溶质质量分数;称量时要注意左物右码;量筒选择需要超过所量取液体的体积且接近性原则;根据电解水的知识进场分析解答即可. |
| 解答: | 解:(1)所需的氢氧化钠质量为100g×10%=10g,故填:10; (2)称量时,氢氧化钠固体应放于天平左盘,量取的水的体积为90ml,故需要选择100ml的量筒,故填:左,100; (3)a管产生的气体较多,是氢气,说明与电源的负极相连,b管产生的是氧气,是用带火星的木条检验,电解水时生成的是氢气和氧气,故填:负,带火星的木条,2H2O (4)电解水时生成了氢气和氧气,说明水中含有氢元素和氧元素,从而说明水是化合物,故填:水分解生成了氢气和氧气; (5)电解后水的质量减小,溶质不变,溶质质量分数增大,故填:>. |
| 点评: | 本题考查了水的有关知识,完成此题,可以依据已有的知识进行. |

维生素C(C6H8O6)是人体不可缺少的营养物质。下列说法错误的是
A.维生素C不属于氧化物 B.维生素C 中碳、氧元素质量比为1∶1
C.维生素C能增强人体抗病能力 D.新鲜水果和蔬菜中富含维生素C
用灯帽盖灭酒精灯的灭火原理是( )
|
| A. | 清除可燃物 | B. | 降低酒精的着火点 |
|
| C. | 隔绝空气 | D. | 降低温度至酒精的着火点以下 |
形成酸雨的主要物质是( )
|
| A. | 粉尘 | B. | 一氧化碳 | C. | 甲烷 | D. | 二氧化硫 |
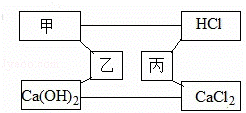
图中甲、乙、丙是初中化学常见的物质,用“﹣”连接的两种物质在溶液中可发生化学反应,下列说法不正确的是( )
|
| A. | 甲可以为盐 | B. | 乙只能是氧化物或酸 |
|
| C. | 丙只能是金属单质、盐或碱 | D. | 其中一个反应能同时生成两种沉淀 |
 2H2↑+O2↑;
2H2↑+O2↑;