题目内容
11.密闭容器内含有4种物质,在一定条件下充分反应测得反应前后各物质的质量如下表所示:已知A与C的相对分子质量之比为197:158,下列推理正确的是( )| 物质 | A | B | C | D |
| 反应前的质量/g | 19.7 | 8.7 | 31.6 | 0.4 |
| 反应后的质量/g | 待测 | 17.4 | 0 | 3.6 |
| A. | A、B是反应物,C、D是生成物 | |
| B. | 反应过程中,B与D变化的质量之比为87:43 | |
| C. | 反应后密闭容器中A的质量为19.7g | |
| D. | 反应中A与C的化学计量数之比为1:2 |
分析 反应后B质量增加8.7g,是生成物;
反应后C质量减小31.6g,是反应物;
反应后D质量增加3.2g,是生成物;
根据质量守恒定律可知,A是生成物,生成的质量为:31.6g-8.7g-3.2g=19.7g.
解答 解:A、C是反应物,ABD为生成物,该选项说法不正确;
B、反应过程中,B与D变化的质量比为:8.7g:3.2g=87:32,该选项说法不正确;
C、反应后密闭容器中A的质量为:19.7g+19.7g=39.4g,该选项说法不正确;
D、设A与C的化学计量数之比为x:y,则有:197x:158y=19.7g:31.6g,x:y=1:2,该选项说法正确.
故选:D.
点评 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础

练习册系列答案
相关题目
6.下列有关金属和合金的说法,错误的是( )
| A. | 金属大多呈银白色且有良好的导电性和延展性 | |
| B. | 合金的很多性能与组成它们的纯金属不同 | |
| C. | 青铜器表面的绿色物质主要成分是【Cu2(OH)2CO3】,可推测铜生锈是铜与水、氧气共同作用的结果 | |
| D. | 铝在空气中表面生成致密的氧化铝薄膜,使铝具有很好的抗腐蚀性能 |
16. “五一”假期,小兵对“金属与酸反应快慢的影响因素”进行了探究.
“五一”假期,小兵对“金属与酸反应快慢的影响因素”进行了探究.
【提出问题】金属与酸反应的快慢受哪些因素的影响呢?
【猜想与假设】a.可能与酸的质量分数有关;b.可能与金属的形状有关;
c.可能与金属的种类有关
【设计并实验】小兵进行如下实验.(3分钟时反应均未结束)
(1)写出稀硫酸与铁反应的化学方程式Fe+H2SO4=FeSO4+H2↑.
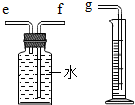
(2)小兵用如图装置收集并测量氢气的体积,其中量筒的作用是根据进入量筒中水的体积,判断生成氢气的体积,氢气应从e(填e或f或g)管通入.
【收集证据】
(3)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是②④
【得出结论】
(4)结论是酸的质量分数越大,反应速率越快.金属与酸的接触面积越大,反应速率越快.金属活动性越强反应越快.
【评价与反思】
(5)下表是小兵第①组实验的详细数据.
请描述锌与硫酸反应的快慢的变化并解释原因由慢到快然后逐渐减慢;随着反应的进行,硫酸被消耗,硫酸溶质质量分数变小.
(6)金属与酸反应的快慢可能还受哪些因素影响?设计实验验证温度;取质量相等的锌粒分别放入两只试管中,然后分别加入溫度不同,形状、体积和溶质质量分数相同的稀硫酸,测量收集等体积的氢气所需要的时间.
 “五一”假期,小兵对“金属与酸反应快慢的影响因素”进行了探究.
“五一”假期,小兵对“金属与酸反应快慢的影响因素”进行了探究.【提出问题】金属与酸反应的快慢受哪些因素的影响呢?
【猜想与假设】a.可能与酸的质量分数有关;b.可能与金属的形状有关;
c.可能与金属的种类有关
【设计并实验】小兵进行如下实验.(3分钟时反应均未结束)
| 实验 编号 | 硫酸的质量分数 (均取20mL) | 金属 (均取2g) | 金属形状 | 氢气的体积(mL) (均收集3分钟) |
| ① | 20% | 锌 | 粉状 | 61.7 |
| ② | 20% | 铁 | 片状 | 50.9 |
| ③ | 20% | 锌 | 片状 | 55.7 |
| ④ | 30% | 铁 | 片状 | 79.9 |
(2)小兵用如图装置收集并测量氢气的体积,其中量筒的作用是根据进入量筒中水的体积,判断生成氢气的体积,氢气应从e(填e或f或g)管通入.
【收集证据】
(3)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是②④
【得出结论】
(4)结论是酸的质量分数越大,反应速率越快.金属与酸的接触面积越大,反应速率越快.金属活动性越强反应越快.
【评价与反思】
(5)下表是小兵第①组实验的详细数据.
| 时段(均为1分钟) | 第1分钟 | 第2分钟 | 第3分钟 | 第4分钟 | 第5分钟 | 第6分钟 |
| H2的体积 | 13.1mL | 26.7mL | 21.9mL | 9.6mL | 7.6mL | 6.0mL |
(6)金属与酸反应的快慢可能还受哪些因素影响?设计实验验证温度;取质量相等的锌粒分别放入两只试管中,然后分别加入溫度不同,形状、体积和溶质质量分数相同的稀硫酸,测量收集等体积的氢气所需要的时间.
3.除去下表物质中含有的杂质,所选试剂或方法错误的是( )
| 选 项 | 物 质 | 杂 质 | 除去杂质所选试剂或方法 |
| A | 碳粉 | 氧化铁 | 稀硫酸 |
| B | 碳酸钠 | 碳酸氢钠 | 加热 |
| C | 硫酸铜溶液 | 硫酸 | 加入适量氢氧化铜 |
| D | 硝酸铜溶液 | 硫酸铜 | 氯化钡溶液 |
| A. | A | B. | B | C. | C | D. | D |
20.某密闭容器中有W、氧气和二氧化碳三种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表.根据表中信息,判断下列说法正确的是( )
| 物质 | W | O2 | CO2 | H2O |
| 反应前质量/g | 16 | 70 | 1 | 0 |
| 反应后质量/g | 0 | 待测 | 45 | 36 |
| A. | 该反应可能是氧化反应 | |
| B. | W中一定含有碳、氢两种元素,质量比为3:1 | |
| C. | W中一定含有碳、氢两种元素,可能含有氧 | |
| D. | 反应生成的CO2和H2O的质量比为45:36 |
1.下列实验操作正确的是( )
| A. | 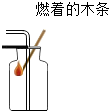 二氧化碳验满 | B. | 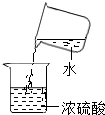 稀释浓硫酸 | C. |  给液体加热 | D. |  测溶液pH |
