题目内容
14.生活中 常接触到“碘盐”、“加铁酱油”等物品,这里的“碘”、“铁”指的是( )| A. | 分子 | B. | 原子 | C. | 元素 | D. | 单质 |
分析 “碘盐”、“加铁酱油”等物品,这里的“碘”、“铁”等不是以单质、分子、原子等形式存在,而是指元素,通常用元素及其所占质量(质量分数)来描述.
解答 解:“碘盐”、“加铁酱油”等物品,这里的“碘”、“铁”等不是以单质、分子、原子等形式存在,这里所指的“碘”、“铁”是强调存在的元素,与具体形态无关.
故选:C.
点评 本题难度不大,主要考查元素与微观粒子及物质的区别,加深对元素概念的理解是正确解答此类试题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.如图是元素周期表中铁、氧两种元素的相关信息,下列有关说法正确的是( )
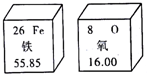

| A. | 氧原子的核外电子数为8 | |
| B. | 铁元素和氧元素都属于非金属元素 | |
| C. | 铁的相对原子质量是55.85g | |
| D. | 铁元素与氧元素只能组成一种化合物 |
9.某实验小组在探究碱的化学性质实验时,用到了氢氧化钠溶液和氢氧化钙溶液.
(1)甲同学不小心将这两种溶液混合在一起,结果产生白色沉淀的现象,说明氢氧化钠溶液变质了.写出变质时发生反应的化学方程式2NaOH+CO2=Na2CO3+H2O.
(2)同学们对变质的氢氧化钠溶液中溶质的成分产生了兴趣,进行如下探究:
【提出问题】氢氧化钠溶液中溶质的成分是什么?
【做出猜想】猜想一:Na2CO3
猜想二:Na2CO3和NaOH(写化学式)
【进行讨论】甲同学取少量待测液加入足量的稀盐酸,有气泡产生.认为猜想一成立.乙同学不同意甲同学的观点,理由是猜想二中也含有碳酸钠,加入足量的盐酸也能产生气泡.
【设计实验】请你验证猜想二成立,并完成实验报.
【反思评价】在实验室中,氢氧化钠应密封保存.
(1)甲同学不小心将这两种溶液混合在一起,结果产生白色沉淀的现象,说明氢氧化钠溶液变质了.写出变质时发生反应的化学方程式2NaOH+CO2=Na2CO3+H2O.
(2)同学们对变质的氢氧化钠溶液中溶质的成分产生了兴趣,进行如下探究:
【提出问题】氢氧化钠溶液中溶质的成分是什么?
【做出猜想】猜想一:Na2CO3
猜想二:Na2CO3和NaOH(写化学式)
【进行讨论】甲同学取少量待测液加入足量的稀盐酸,有气泡产生.认为猜想一成立.乙同学不同意甲同学的观点,理由是猜想二中也含有碳酸钠,加入足量的盐酸也能产生气泡.
【设计实验】请你验证猜想二成立,并完成实验报.
| 实验操作 | 实验现象 | 实验结论 |
| ①取一定量的待测液于试管中,加入过量的氯化钙溶液. ②充分反应后静置,取上层淸液加入无色酚酞溶液 | 产生白色沉淀 无色酚酞溶液变红 | 猜想二成立 |
6.下列物质的转化属于物理变化的是( )
| A. | 纯碱→烧碱 | B. | 生石灰→熟石灰 | C. | 石墨→金刚石 | D. | 二氧化碳→干冰 |
3.我国制碱工业的先驱侯德榜将制碱与制氨结合起来的联合制碱法,为纯碱和氮肥工业技术的发展做出了杰出的贡献.其生产工艺流程示意图如图1所示:
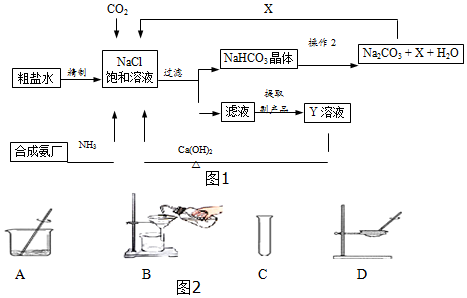
(1)粗盐水中主要含有Ca2+、Mg2+、SO42-等杂质离子,工业上常用加入稍过量的①NaOH溶液、②Na2CO3溶液、③BaCl2溶液及适量的盐酸等除杂、精制.则加入试剂合理的顺序为BC(填字母序号).
A.①②③B.③②①C.①③②
(2)加盐酸的作用是(用方程式表示)NaOH+HCl═NaCl+H2O、Na2CO3+2HCl=2NaCl+H2O+CO2↑.
(3)制碱原理可看作是由①CO2+NH3+H2O=NH4HCO3和②NaCl+NH4HCO3=NaHCO3+NH4Cl两个反应加合而成.反应②为复分解反应,请根据复分解反应发生的条件及表1中相关物质20℃时的溶解度,分析反应②为何能顺利进行?相同条件下,NaHCO3的溶解度较小.
表 相关物质的溶解度(20℃)(单位:g)
(4)操作2为洗涤、煅烧.晶体应在如图2所示装置B中(填字母序号)进行“洗涤”操作.
在上述操作中,如何判断晶体已经洗涤干净取最后一次洗涤液,滴加硝酸银溶液,若没有沉淀则已洗涤干净.
(5)X的化学式为CO2,若X直接排放到空气中会造成的后果是温室效应.
(6)Y是滤液中最主要成分,Y与Ca(OH)2反应的产物之一可用于循环使用,该产物的名称为氨气,Y的化学式为NH4Cl,写出Y的一种用途用作氮肥.

(1)粗盐水中主要含有Ca2+、Mg2+、SO42-等杂质离子,工业上常用加入稍过量的①NaOH溶液、②Na2CO3溶液、③BaCl2溶液及适量的盐酸等除杂、精制.则加入试剂合理的顺序为BC(填字母序号).
A.①②③B.③②①C.①③②
(2)加盐酸的作用是(用方程式表示)NaOH+HCl═NaCl+H2O、Na2CO3+2HCl=2NaCl+H2O+CO2↑.
(3)制碱原理可看作是由①CO2+NH3+H2O=NH4HCO3和②NaCl+NH4HCO3=NaHCO3+NH4Cl两个反应加合而成.反应②为复分解反应,请根据复分解反应发生的条件及表1中相关物质20℃时的溶解度,分析反应②为何能顺利进行?相同条件下,NaHCO3的溶解度较小.
表 相关物质的溶解度(20℃)(单位:g)
| NaCl | NH4HCO3 | NaHCO3 | NH4Cl |
| 36.0 | 21.7 | 9.6 | 37.2 |
在上述操作中,如何判断晶体已经洗涤干净取最后一次洗涤液,滴加硝酸银溶液,若没有沉淀则已洗涤干净.
(5)X的化学式为CO2,若X直接排放到空气中会造成的后果是温室效应.
(6)Y是滤液中最主要成分,Y与Ca(OH)2反应的产物之一可用于循环使用,该产物的名称为氨气,Y的化学式为NH4Cl,写出Y的一种用途用作氮肥.