题目内容
用镁和铁分别跟足量的稀硫酸充分反应,得到质量相同的氢气.则参加反应的镁和铁的质量比为 (最简比值).
考点:金属的化学性质,根据化学反应方程式的计算
专题:金属与金属材料
分析:镁和铁两种金属分别跟足量的稀硫酸反应的化学方程式为:Mg+H2SO4=MgSO4+H2↑,Fe+H2SO4=FeSO4+H2↑,由此可知,产生的氢气来源于硫酸中的氢离子,故参与反应的镁和铁质量符合得到相同质量氢气的条件.据此分析解答即可;根据金属活动性顺序表中,排在氢前面的金属和酸反应产生氢气,排在氢后面的金属和酸反应不能产生氢气来解答.
解答:解:假设Mg、Fe两种金属分别跟稀硫酸充分反应,得到氢气的质量都是2g,
设参与反应的Mg的质量为x,Al为y,
Mg+2H2SO4=MgSO4+H2↑,Fe+H2SO4=FeSO4+H2↑
24 2 56 2
x 2g y 2g
则
=
,
=
,解得x=24g,y=56g
故Mg、Fe质量比为:24g:56g=3:7
故答案:3:7.
设参与反应的Mg的质量为x,Al为y,
Mg+2H2SO4=MgSO4+H2↑,Fe+H2SO4=FeSO4+H2↑
24 2 56 2
x 2g y 2g
则
| 24 |
| 2 |
| x |
| 2g |
| 56 |
| 2 |
| y |
| 2g |
故Mg、Fe质量比为:24g:56g=3:7
故答案:3:7.
点评:本题主要是利用化学方程式和假设法相结合方式解答问题,从此题可以看出在利用化学方程式解答问题时,运用假设法,对解决一些复杂的问题有很大帮助.

练习册系列答案
相关题目
下列是纯净的氢气在空气中燃烧现象的描述,其中正确的是( )
①产生淡蓝色火焰 ②放出大量的热 ③生成水.
①产生淡蓝色火焰 ②放出大量的热 ③生成水.
| A、①② | B、②③ | C、①③ | D、①②③ |
小明将带火星的木条插入一瓶无色气体中,木条剧烈燃烧.该气体可能是( )
| A、空气 | B、氧气 |
| C、氮气 | D、二氧化碳 |
下列各组物质中,在常温下能发生化学反应的是( )
| A、硫和氧气 |
| B、氯酸钾和二氧化锰 |
| C、铜和硝酸汞溶液 |
| D、氧化铜和木炭 |
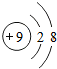 ,则该离子带
,则该离子带