题目内容
实验室常用过氧化钠与水反应制取氧气,反应的化学方程式如下:2Na2O2+2H2O═4NaOH+O2↑,试计算:
(1)15.6g过氧化钠与足量的水反应可以生成多少克氧气?
(2)标准状况下,氧气的密度约为1.43g/L,多少空气中才可能含有这么多氧气.(计算结果保留到0.1)
(1)15.6g过氧化钠与足量的水反应可以生成多少克氧气?
(2)标准状况下,氧气的密度约为1.43g/L,多少空气中才可能含有这么多氧气.(计算结果保留到0.1)
考点:根据化学反应方程式的计算,空气的成分及各成分的体积分数
专题:有关化学方程式的计算
分析:(1)根据反应化学方程式,利用已知量(过氧化钠质量)计算生成氧气的质量进行解答;
(2)根据氧气的质量求出氧气的体积,从而计算出空气的体积进行解答.
(2)根据氧气的质量求出氧气的体积,从而计算出空气的体积进行解答.
解答:解:(1)设生成O2的质量为x
2Na2O2+2H2O═4NaOH+O2↑
156 32
15.6g x
=
解得x=3.2g
(2)标准状况下,氧气的体积=
=2.24L
空气的体积=
=10.7L
答:(1)15.6g过氧化钠与足量的水反应可以生成3.2g氧气;
(2)标准状况下,10.7L空气中才可能含有这么多氧气.
2Na2O2+2H2O═4NaOH+O2↑
156 32
15.6g x
| 156 |
| 15.6g |
| 32 |
| x |
解得x=3.2g
(2)标准状况下,氧气的体积=
| 3.2g |
| 1.43g/L |
空气的体积=
| 2.24L |
| 21% |
答:(1)15.6g过氧化钠与足量的水反应可以生成3.2g氧气;
(2)标准状况下,10.7L空气中才可能含有这么多氧气.
点评:根据反应的化学方程式进行计算时,所使用的物质的质量必须为完全反应的物质的质量,未参加反应的物质质量不能代入化学方程式进行计算.

练习册系列答案
相关题目
下列各组的主要成分都可用CaCO3表示的是( )
| A、生石灰、石灰石 |
| B、石灰石、大理石 |
| C、生石灰、石灰水 |
| D、石灰浆、石灰水 |
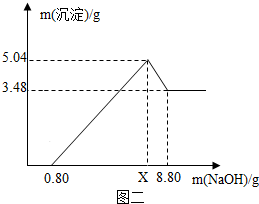
 A、B、C三种固体物质的溶解度如右图所示,根据图答题:
A、B、C三种固体物质的溶解度如右图所示,根据图答题: