题目内容
15.碳和部分碳的化合物间转化关系如图所示.
(1)物质X的化学式为CO.
(2)在物质的分类中,Y属于B.
A.单质 B.化合物 C.氧化物 D.混合物
(3)写出一种符合题意的Y与盐酸反应的方程式CaCO3+2HCl=CaCl2+H2O+CO2↑.
(4)写出X的一种工业用途冶炼金属.
分析 由于是碳和碳的化合物之间的转化关系,所以X一定也是含碳物质,由于其能够与二氧化碳之间时间相互转化,并且由碳生成,所以应该为一氧化碳.题目要求书写的化学方程式按照给定的要求实现转化关系即可.
解答 解:分析题中所给出的图,可以看出其中有一个C、CO2、X的三角关系图,回顾所学知识,符合这样的三角关系图为C、CO2和CO的关系,则可知X为CO;又Y与HCl反应可制得CO2,则Y必为碳酸盐类物质.
(1)X与二氧化碳之间进行相互转化,并由碳生成,故X为CO;故填:CO;
(2)Y与稀盐酸反应生成二氧化碳气体,故Y属于碳酸盐,属于化合物;故填:B;
(3)碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,故填:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(4)一氧化碳具有可燃性和还原性,可以作燃料或冶炼金属的还原剂;故填:冶炼金属.
点评 熟悉碳及碳的化合物之间的转化关系,在初中物质推断中用到的较为普遍.平时注意借助知识网络整合知识、梳理知识.

练习册系列答案
相关题目
10.在一个密闭容器里有X、Y、Z、Q四种物质,在一定条件下充分反应,测得反应前后各物质的质量如表:
下列说法中,错误的是( )
| 物质 | X | Y | Z | Q |
| 反应前质量/g | 4 | 10 | 1 | 25 |
| 反应后质量/g | 待测 | 21 | 6 | 9 |
| A. | 该反应为化合反应 | B. | 该反应遵循质量守恒定律 | ||
| C. | X中待测值为4 | D. | 该反应中X可能是催化剂 |
20.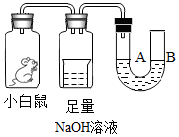 根据如图来回答:经数小时后,U形管A、B两处的液面会出现下列哪种情况(①假设实验装置足以维持实验过程中小白鼠的生命活动;②瓶口密封且忽略水蒸气和温度变化对实验结果的影响;③NaOH溶液可完全吸收二氧化碳气味)( )
根据如图来回答:经数小时后,U形管A、B两处的液面会出现下列哪种情况(①假设实验装置足以维持实验过程中小白鼠的生命活动;②瓶口密封且忽略水蒸气和温度变化对实验结果的影响;③NaOH溶液可完全吸收二氧化碳气味)( )
 根据如图来回答:经数小时后,U形管A、B两处的液面会出现下列哪种情况(①假设实验装置足以维持实验过程中小白鼠的生命活动;②瓶口密封且忽略水蒸气和温度变化对实验结果的影响;③NaOH溶液可完全吸收二氧化碳气味)( )
根据如图来回答:经数小时后,U形管A、B两处的液面会出现下列哪种情况(①假设实验装置足以维持实验过程中小白鼠的生命活动;②瓶口密封且忽略水蒸气和温度变化对实验结果的影响;③NaOH溶液可完全吸收二氧化碳气味)( )| A. | A处上升,B处下降 | B. | A、B两处都下降 | C. | A处下降,B处上升 | D. | A、B两处都不变 |
4.研究小组进行木炭还原氧化铁的探究活动.将木炭、氧化铁及试管充分烘干,并将木炭和氧化铁混合均匀、研磨.取适量上述混合物于试管中,用右图1所示的装置加热(试管竖直向上,可使加热时的热量尽少散失).
【提出问题】实验结束后,试管中的剩余固体X含有哪些成分,质量分别是多少?
【查阅资料】
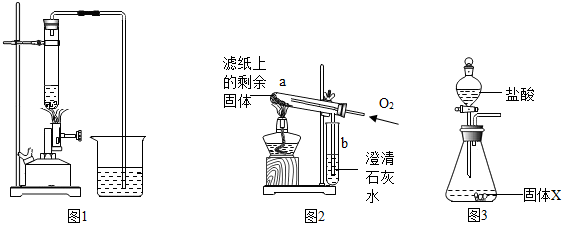
铁的氧化物被还原时,是从高价铁的氧化物逐级还原成低价铁的氧化物,最后还原成金属铁.铁的部分氧化物的性质如下:
Fe3O4具有很好的磁性,能被磁铁吸引.铁的三种氧化物均不溶于水,但能溶于稀盐酸,分别发生如下反应:
Fe2O3+6HCl══2FeCl3+3H2O
Fe3O4+8HCl══2FeCl3+FeCl2+4H2O
FeO+2HCl══FeCl2+H2O
黄色的FeCl3溶液中滴入无色的KSCN溶液,溶液变为红色,该实验常用于检验FeCl3;FeCl3溶液遇单质铁发生反应:2FeCl3+Fe=3FeCl2,溶液变为浅绿色.
【猜想】固体X可能含有:①Fe ②FeO ③Fe3O4 ④Fe2O3(写化学式) ⑤C
【实施实验】
目的:确定固体X的组成.
【反思改进】
同学们讨论发现,用上述实验方法不能确定固体X中一定没有Fe3O4,理由是固体X中如果含有Fe3O4,步骤V中加盐酸后,由于铁与FeCl3反应生成FeCl2,遇KSCN溶液也不变血红色.
为确定固体X中是否含Fe3O4并测定其中各成分的质量,同学们又进行了以下实验:
【获得结论】
(1)为确定固体X中是否含Fe3O4,m1~m4中应该用到的数据有m1、m2、m3和m4.
(2)固体X各成分的质量比为11:168.
【提出问题】实验结束后,试管中的剩余固体X含有哪些成分,质量分别是多少?
【查阅资料】

铁的氧化物被还原时,是从高价铁的氧化物逐级还原成低价铁的氧化物,最后还原成金属铁.铁的部分氧化物的性质如下:
Fe3O4具有很好的磁性,能被磁铁吸引.铁的三种氧化物均不溶于水,但能溶于稀盐酸,分别发生如下反应:
Fe2O3+6HCl══2FeCl3+3H2O
Fe3O4+8HCl══2FeCl3+FeCl2+4H2O
FeO+2HCl══FeCl2+H2O
黄色的FeCl3溶液中滴入无色的KSCN溶液,溶液变为红色,该实验常用于检验FeCl3;FeCl3溶液遇单质铁发生反应:2FeCl3+Fe=3FeCl2,溶液变为浅绿色.
【猜想】固体X可能含有:①Fe ②FeO ③Fe3O4 ④Fe2O3(写化学式) ⑤C
【实施实验】
目的:确定固体X的组成.
| 步骤 | 操作 | 主要现象 | 结论 |
| I | 取部分冷却后的固体X倒在滤纸上,用磁铁充分吸引. | 部分固体被吸引到磁铁上 | 可能有Fe或Fe3O4 |
| II | 取滤纸上的剩余固体少量,放入图2所示的试管a中,通入氧气,用酒精灯加热. | 固体剧烈燃烧,b中溶液变浑浊 | 一定有C. |
| III | 另取滤纸上的剩余固体少量,放入试管中,加入足量的稀盐酸. | 无明显现象 | 一定没有FeO和Fe2O3 . |
| IV | 取步骤I磁铁上的固体少量,放入试管中,逐滴加入稀盐酸. | 产生产生气泡. | 一定有Fe |
| V | 在步骤IV所得溶液中逐滴加入KSCN溶液. | 溶液不变红色 | 一定没有Fe3O4 |
同学们讨论发现,用上述实验方法不能确定固体X中一定没有Fe3O4,理由是固体X中如果含有Fe3O4,步骤V中加盐酸后,由于铁与FeCl3反应生成FeCl2,遇KSCN溶液也不变血红色.
为确定固体X中是否含Fe3O4并测定其中各成分的质量,同学们又进行了以下实验:
| 步骤 | 操作 | 数据 |
| I | 重新取部分冷却至室温的固体X,称量其质量为m1. | m1=17.9g |
| II | 将称量好的固体X全部放入图3所示的锥形瓶中,称量整套装置及药品的质量为m2;打开分液漏斗旋塞,放入足量稀盐酸后关闭旋塞,待没有气泡产生并恢复至室温,再次称量整套装置及药品的质量为m3. | m2=317.9g m3=317.3g |
| III | 将锥形瓶中剩余的固体过滤、洗涤并干燥,称量其质量为m4. | m4=1.1g |
(1)为确定固体X中是否含Fe3O4,m1~m4中应该用到的数据有m1、m2、m3和m4.
(2)固体X各成分的质量比为11:168.
5.2016年10月17,中国发射“神舟十一号”载人飞船,将与“天宫二号”在太空会合.发射“神舟十一号”飞船的“长征二号F”运载火箭在升空时将会发生下列变化,其中属于化学变化的是( )
| A. | 火箭点火 | B. | 导流槽内的水受热汽化 | ||
| C. | 隔热材料脱落 | D. | 整流罩脱落 |

 据新闻报道某城镇边的一条河中惊现红色河水,被称为“红色多瑙河”,原来是某印染厂将积存的印染废水趁大雨倒入河水中,造成水体污染.
据新闻报道某城镇边的一条河中惊现红色河水,被称为“红色多瑙河”,原来是某印染厂将积存的印染废水趁大雨倒入河水中,造成水体污染.