题目内容
7.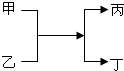 甲、乙、丙、丁均为初中化学常见物质,它们有如图的转化关系,请回答:
甲、乙、丙、丁均为初中化学常见物质,它们有如图的转化关系,请回答:(1)若甲和乙反应生成的丙为最清洁的气体燃料,则丙的化学式为H2;其中甲是常见金属,则此化学反应的基本类型为置换反应.
(2)若乙是能够支持燃烧的气体,请写出在一定条件下符合此转化关系的一个化学方程式CH4+2O2 $\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O或C2H5OH+3O2 $\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O等.
(3)若甲是极易与血红蛋白结合的有毒气体,丙是常见金属,如果人体缺丙元素,易患贫血.工业上冶炼该金属的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(4)若甲为气体,并能与乙的溶液反应生成白色沉淀.请写出在一定条件下符合此转化关系的一个化学方程式CO2+Ca(OH)2═CaCO3↓+H2O(合理即可).
分析 根据题干提供的信息进行分析,丙为最清洁的气体燃料,则丙是氢气,可以通过活泼金属与酸发生置换反应,若乙是能够支持燃烧的气体,则乙是一氧化碳,甲是极易与血红蛋白结合的有毒气体,则甲是一氧化碳,具有还原性,能还原金属氧化物,二氧化碳能够和石灰水反应产生沉淀等,据此分析解答即可.
解答 解:(1)最清洁的气体燃料是氢气,该过程为金属与酸反应产生氢气,其化学方程式为 Zn+H2SO4 ═ZnSO4+H2↑;该反应是单质和化合物的反应产生新的单质和新的化合物,属于置换反应;
(2)能支持燃烧的气体是氧气,物质在氧气中燃烧生成两种物质,如CH4+2O2 $\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O或C2H5OH+3O2 $\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O等都可以出现这样的变化过程;
(3)若甲是极易与血红蛋白结合的有毒气体,则甲为一氧化碳,丙是我国春秋战国时期就开始生产和使用的一种金属,则丙是铁,则工业上冶炼该金属的化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(4)甲为气体,并能与乙的溶液反应生成白色沉淀,因此可以是二氧化碳和氢氧化钙的反应,氢氧化钙和二氧化碳反应生成碳酸钙和水,反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O(合理即可).
故答案为:(1)H2;置换反应;(2)CH4+2O2 $\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O或C2H5OH+3O2 $\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O等;(3)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;(4)CO2+Ca(OH)2═CaCO3↓+H2O(合理即可).
点评 本题为框图式物质推断题,完成此题,关键是根据题干叙述,找准解题的突破口,直接得出有关物质的化学式,然后根据物质的性质结合框图得出其他物质的化学式.

| A. | 3S表示3个硫元素或3个硫原子 | |
| B. | 氦气的化学式是He | |
| C. | $\underset{N}{•}$H4$\underset{N}{•}$O3中前后氮元素的化合价相同 | |
| D. | 6Fe2+表示6个铁离子 |
| A. | 运输时注意密封 | B. | 贮存时不能受潮或暴晒 | ||
| C. | 与草木灰混合施用 | D. | 施用后立即盖上 |
| A. | 衣服晾干 | B. | 冰雪融化 | C. | 玻璃破碎 | D. | 纸张燃烧 |
| A. | 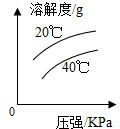 表示氧气的溶解度 | |
| B. | 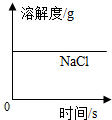 表示恒温蒸发一定量的氯化钠溶液 | |
| C. | 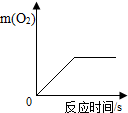 表示加热一定量的高锰酸钾 | |
| D. | 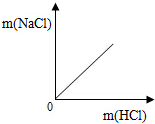 表示向一定量氢氧化钠溶液中滴加稀盐酸 |
| A. | 盛放石灰水的试剂瓶 | |
| B. | 用一氧化碳还原氧化铁后的硬质玻璃管 | |
| C. | 一氧化碳还原氧化铜后,附有红色固体残渣的试管 | |
| D. | 盛放过生锈铁钉后留下红棕色固体的烧杯 |
| A. | 发生重金属盐中毒时,可先服用大量的鲜豆浆、牛奶等缓解中毒症状、再去就医 | |
| B. | 对于甲状腺肿大患者来说,应在饮食上适当食用海产品等含碘丰富的食物 | |
| C. | 健康人体血浆的正常pH范围为:7.53~7.54 | |
| D. | 霉变的粮食经淘洗、蒸煮后,即可放心食用,不会危害人体健康 |
