题目内容
19. 如图是某品牌补铁剂的标签.请回答:
如图是某品牌补铁剂的标签.请回答:(1)富马酸亚铁含有4种元素,富马酸亚铁中C:H的原子个数比为2:1.
(2)富马酸亚铁中C、H元素的质量比为24:1;
(3)已知富马酸亚铁(C4H2FeO4)中铁元素的质量分数为33%,若每次服用1包该补铁剂,摄入铁元素的质量为66mg.
分析 (1)根据富马酸亚铁化学式的含义,进行分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据题意,已知富马酸亚铁(C4H2FeO4)中铁元素的质量分数为33%,每包含富马酸亚铁0.2g,每次服用1包该补铁剂,据此结合化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答 解:(1)富马酸亚铁是由碳、氢、铁、氧四种元素组成的;一个富马酸亚铁分子中含有4个碳原子、2个氢原子,则富马酸亚铁中C:H的原子个数比为4:2=2:1
(2)富马酸亚铁中C、H元素的质量比为(12×4):(1×2)=24:1.
(3)已知富马酸亚铁(C4H2FeO4)中铁元素的质量分数为33%,每包含富马酸亚铁0.2g,每次服用1包该补铁剂,摄入铁元素的质量为0.2g×1×33≈0.066g=66mg.
故答案为:(1)2:1;(2)24:1;(3)66.
点评 本题难度不大,考查同学们结合标签新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
11.下列有关盐酸溶液的说法正确的是( )
| A. | 该溶液是纯净物 | |
| B. | 该溶液上层的密度小,下层的密度大 | |
| C. | 该溶液的溶质是气体 | |
| D. | 镁、铁、铜都能与稀盐酸反应 |
8.研究氢氧化钠性质实验中的部分实验及现象记录如下,其中现象不合理的是( )
| 序号 | 实 验 | 现 象 |
| A | 将NaOH固体放在表面皿上,放置一会儿 | 固体受潮,逐渐溶解 |
| B | 向盛有NaOH溶液的试管中滴入无色酚酞试液 | 溶液变红 |
| C | 向盛有NaOH溶液的试管中滴加稀HCl | 有NaCl生成 |
| D | 向盛有NaOH溶液的试管中滴加 CuSO4溶液 | 产生蓝色(絮状)沉淀 |
| A. | A | B. | B | C. | C | D. | D |


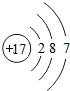 ,该元素的原子在化学反应中比较容易得到(填“得到”或“失去”)电子变成阴(填“阴”或“阳”)离子,形成的离子符号为Cl-.
,该元素的原子在化学反应中比较容易得到(填“得到”或“失去”)电子变成阴(填“阴”或“阳”)离子,形成的离子符号为Cl-.