题目内容
 水是生命之源,人类的生活生产离不开水.
水是生命之源,人类的生活生产离不开水.(1)自来水属于
(2)某同学收集到一杯有臭味的混浊污水,先用滤纸进行过滤,过滤时所用的玻璃仪器有烧杯、玻璃棒和
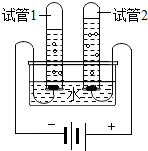
(3)该同学为了探究水的组成,做了水的电解实验,如图所示.用化学方程式表示其实验原理:
考点:硬水与软水,过滤的原理、方法及其应用,电解水实验,纯净物和混合物的判别,书写化学方程式、文字表达式、电离方程式
专题:空气与水
分析:物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成;纯净物是由一种物质组成.硬水是指含有较多钙镁离子的水,软水是指含有较少钙镁离子的水.区分硬水和软水的方法是:用肥皂水或加热的方法,如果水的硬度比较大时,就会产生大量的水垢.过滤用到的仪器有:铁架台、烧杯、玻璃棒和漏斗;活性炭具有吸附作用.水在通电的条件下生成氢气和氧气,并且是正氧负氢,化学反应前后元素的种类不变.
解答:解:(1)自来水含有水和矿物质,属于混合物;区分硬水和软水的方法是:用肥皂水或加热的方法;故答案为:混合物;肥皂水;加热煮沸
(2)过滤用到的仪器有:铁架台、烧杯、玻璃棒和漏斗;活性炭具有吸附作用;故答案为:漏斗;用活性炭吸附
(3)水在通电的条件下生成氢气和氧气,电解水反应式是:2H2O
2H2↑+O2↑.并且是正氧负氢,根据化学反应前后元素的种类不变,证明水的组成.实际观察到的现象是正负两极气体的体积比小于1:2的原因有:氧气比氢气更易溶于水,装置漏气,一部分氧气与电极反应.
故答案为:2H2O
2H2↑+O2↑;氢气;化学反应前后元素的种类不变;氧气比氢气更易溶于水
(2)过滤用到的仪器有:铁架台、烧杯、玻璃棒和漏斗;活性炭具有吸附作用;故答案为:漏斗;用活性炭吸附
(3)水在通电的条件下生成氢气和氧气,电解水反应式是:2H2O
| ||
故答案为:2H2O
| ||
点评:本考点考查了物质的分类、水的净化、水的电解等,属于结合课本知识的信息,也体现了化学反应的实质.还结合了新课标中的一个新的考点硬水与软水的区分,一定要加强记忆,综合应用.本考点主要出现在填空题和选择题中.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
下列物质中,含有氧气分子的是( )
| A、二氧化碳 | B、液态空气 |
| C、水 | D、臭氧 |
乙烯(C2H4)是石油炼制的重要产物之一,常温常压时,乙烯是一种气体,它与另一种气体组成的混合物中碳元素的质量分数为87%,则另一种气体可能是( )
| A、C2H2 |
| B、CH4 |
| C、H2 |
| D、C3H6 |
下列说法正确的是( )
| A、空气中氮气的体积分数为21% |
| B、人体中含量最多的元素是水 |
| C、海洋中含量最多的非金属元素是氧元素 |
| D、地壳中含量最多的金属元素是铁元素 |
下列结构示意图中,表示金属原子的是( )
A、 |
B、 |
C、 |
D、 |
