题目内容
乙烯(C2H4)是石油炼制的重要产物之一,常温常压时,乙烯是一种气体,它与另一种气体组成的混合物中碳元素的质量分数为87%,则另一种气体可能是( )
| A、C2H2 |
| B、CH4 |
| C、H2 |
| D、C3H6 |
考点:元素的质量分数计算
专题:化学式的计算
分析:根据物质中某元素的质量分数=
×100%,先计算出乙烯中碳元素的质量百分比为 85.7%,因为,混合气体的碳元素质量分数为87%,而乙烯<87%,所以,另一种气体的含碳量一定要>87%才能是混合气体中碳元素质量分数大于87%,分别计算出选项中碳元素的质量百分比,即可解答.
| 该元素相对原子质量×原子个数 |
| 该物质的相对分子质量 |
解答:解:乙烯中,碳元素的质量百分比=
×100%=85.7%,
A、C2H2中碳元素的质量百分比=
×100%=92.3%;
B、CH4中碳元素的质量百分比=
×100%=75%
C、H2中不含有碳元素,碳元素的质量百分比为0;
D、C3H6中碳元素的质量百分比=
×100%=85.7%
因为,混合气体的碳元素质量分数为87%,而乙烯<87%,所以,另一种气体的含碳量一定要>87% 才能使混合气体中碳元素质量分数大于87%;
故选A.
| 12×2 |
| 12×2+4 |
A、C2H2中碳元素的质量百分比=
| 12×2 |
| 12×2+2 |
B、CH4中碳元素的质量百分比=
| 12 |
| 16 |
C、H2中不含有碳元素,碳元素的质量百分比为0;
D、C3H6中碳元素的质量百分比=
| 12×3 |
| 12×3+1×6 |
因为,混合气体的碳元素质量分数为87%,而乙烯<87%,所以,另一种气体的含碳量一定要>87% 才能使混合气体中碳元素质量分数大于87%;
故选A.
点评:本题考查学生根据物质中某元素的质量分数进行分析解题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
检查装的气密性有下列操作步骤:①用带导管的橡皮塞塞紧烧瓶口;②把导管的一端插入盛在烧杯的水里;③用手掌紧贴烧瓶外壁,使瓶内气体受热膨胀;④把手移开,观察导管里水位是否上升,形成一段水柱;⑤观察导管口是否有气泡冒出.其正确的操作顺序为( )
| A、②①③④⑤ |
| B、①②③④⑤ |
| C、①②③⑤④ |
| D、②①③⑤④ |
下列说法中正确的是( )
| A、氧气可以用来作燃料 |
| B、氨水能使无色酚酞试液变红 |
| C、二氧化碳能使紫色石蕊变红 |
| D、水(H2O)和过氧化氢(H2O2)分子中都含有氢气分子 |
下列物质中,属于氧化物的是( )
| A、高锰酸钾 | B、氧气 | C、水 | D、空气 |
胆矾是一种蓝色晶体,化学式是CuSO4?5H2O,在工业上精炼铜,胆矾受热时易失去结晶水,生成白色的无水硫酸铜,上述对胆矾的叙述中,没有涉及的是( )
| A、物理性质 | B、制法 |
| C、用途 | D、化学性质 |




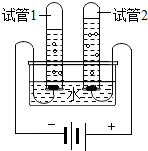 水是生命之源,人类的生活生产离不开水.
水是生命之源,人类的生活生产离不开水.