题目内容
 上完体育课后,小强同学往一瓶矿泉水中加入一片“泡腾片”(其商标部分内容如图所示),立即产生大量气泡,片刻成为一瓶可口的饮料,这引发了身边同学的极大兴趣,于是大家决定对NaHCO3和Na2CO3的热稳定性进行如下的探究:
上完体育课后,小强同学往一瓶矿泉水中加入一片“泡腾片”(其商标部分内容如图所示),立即产生大量气泡,片刻成为一瓶可口的饮料,这引发了身边同学的极大兴趣,于是大家决定对NaHCO3和Na2CO3的热稳定性进行如下的探究:【提出问题】NaHCO3和Na2CO3与盐酸反应都会生成CO2,那两者的热稳定性又如何?
【进行猜想】NaHCO3和Na2CO3的热稳定性差,受热都会发生分解反应.
【设计并进行实验】为验证猜想,同学们设计了 如图装置并进行实验:
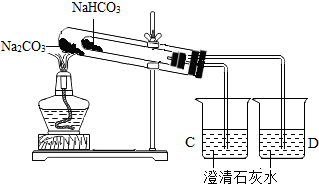
【实验现象】
①装有NaHCO3的小试管内壁有水珠生成.
②烧杯C.D中导管口有气泡冒出,但只有烧杯 C中澄清石灰水变浑浊.
③充分加热后,大试管中的固体无明显变化,小试管中仍有少量白色固体残留.
【实验结论】NaHCO3受热会分解,生成水.
【交流与讨论】根据反应物的组成元素,同学们认为残留的白色固体可能是Na2CO3或
NaOH中的一种,为检验该白色固体,小强设计了如下方案:
Ⅰ.往残留固体中滴加稀盐酸,观察现象,判断白色固体是否为Na2CO3.
Ⅱ.将残留固体溶于水后,滴加无色酚酞试液,判断白色固体是否为NaOH.
同学们经过交流讨论一致认为方案Ⅱ不行,理由是
小强通过方案Ⅰ的实验得出白色固体是Na2CO3,若让你用另一种试剂来验证Na2CO3,你会选用
考点:实验探究物质的性质或变化规律,常见气体的检验与除杂方法,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:【实验结论】根据碳酸氢钠受热分解生成碳酸钠、水和二氧化碳以及二氧化碳能和石灰水反应生成碳酸钙沉淀和水进行解答;
【交流与讨论】根据碳酸氢钠也呈碱性,能使酚酞试液变红进行解答;
根据碳酸钠溶液能和含有钙离子的物质生成反应生成碳酸钙沉淀进行解答.
【交流与讨论】根据碳酸氢钠也呈碱性,能使酚酞试液变红进行解答;
根据碳酸钠溶液能和含有钙离子的物质生成反应生成碳酸钙沉淀进行解答.
解答:解:【实验结论】根据实验现象推断,NaHCO3受热会分解,生成二氧化碳而Na2CO3受热不分解,因此,以上猜想 错误.烧杯C中澄清石灰水变浑浊的反应化学方程式:Ca(OH)2+CO2═CaCO3↓+H2O.
【交流与讨论】Ⅱ:因为碳酸氢钠溶液也是呈碱性的,所以不能根据酚酞变红色来推断一定是氢氧化钠.
根据物质的溶解性可知,鉴别碳酸盐可以用钙离子来检验,所以可以加入氢氧化钙溶液.
故答案为:【实验结论】二氧化碳;错误;Ca(OH)2+CO2═CaCO3↓+H2O;
【交流与讨论】Ⅱ.碳酸钠和氢氧化钠的水溶液都呈碱性,都能使酚酞变红;
Ca(OH)2.
【交流与讨论】Ⅱ:因为碳酸氢钠溶液也是呈碱性的,所以不能根据酚酞变红色来推断一定是氢氧化钠.
根据物质的溶解性可知,鉴别碳酸盐可以用钙离子来检验,所以可以加入氢氧化钙溶液.
故答案为:【实验结论】二氧化碳;错误;Ca(OH)2+CO2═CaCO3↓+H2O;
【交流与讨论】Ⅱ.碳酸钠和氢氧化钠的水溶液都呈碱性,都能使酚酞变红;
Ca(OH)2.
点评:本题通过对“泡腾片”成分的分析,重点考查了钠的两种重要盐碳酸钠和碳酸氢钠的性质、方程式的书写等知识.综合性比较强,解答时要充分利用题目所给的信息.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列变化属于化学变化的是( )
| A、瓷碗破碎 | B、石蜡熔化 |
| C、纸张燃烧 | D、湿衣晾干 |
下列设计的实验方案中不能达到目的是( )
| A、用灼烧闻气味区分羊毛线和棉线 |
| B、用酚酞溶液区分稀盐酸和食盐水 |
| C、用肥皂水区别硬水和软水 |
| D、用尝味道的方法区分厨房中的食盐和蔗糖 |
用括号内物质不能一次性区别开下列各组物质的是( )
| A、CaO、CaCO3、KCl 三种固体(水) |
| B、CaCl2、Na2CO3、K2SO4三种溶液 (Ba(OH)2溶液) |
| C、Cu、Fe、CuO三种固体(稀盐酸) |
| D、CaCl2、Na NO3、K2CO3三种溶液 (Ca(OH)2溶液) |
下列金属中熔点最高的是( )
| A、钨 | B、银 | C、铜 | D、钠 |
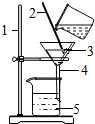 (1)写出图中所示的仪器名称:
(1)写出图中所示的仪器名称: