题目内容
14.如图所示为实验室中常见气体制备、净化、干燥、收集和性质实验的部分仪器(组装实验装置时,可重复选择仪器),某化学小组的同学欲利用其进行下列各探究实验.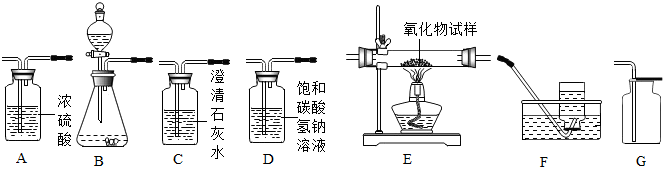
(1)以石灰石和稀盐酸为原料,在晒掩饰中制备并收集干燥、纯净的二氧化碳气体,氨照要求设计实验装置,连接仪器,并检验装置的气密性
①所选仪器的连接顺序为BDAG(从左到右填写仪器序号字母)(提示:挥发出的少量HCl气体可用饱和碳酸氢钠溶液吸收)
②用石灰石和稀盐酸制取二氧化碳的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑
③若将二氧化碳气体通入酚酞试液中,试液显无色.
(2)用一氧化碳气体(含少量水蒸气)测定某铁的氧化物(FexOy)的元素组成比例,并验证反应中气体生成物的性质.所选仪器按A1-----E-----C-----A2顺序连接(A1、A22为浓硫酸洗气瓶),并检验装置的气密性,所设计的实验装置中气体流向是从左向右.
①反应前大玻璃管中加入铁的粉末状氧化物(FexOy)样品的质量为 ag,实验结束后,继续通入一氧化碳气体,直至大玻璃管冷却.这时测量到 E 处大玻璃管中粉末状固体的质量减少了bg,试推算该铁的氧化物的化学式中 x、y 的比值:$\frac{x}{y}$=$\frac{2(a-b)}{7a}$.(用含 a 和 b 的代数式表示).(设所发生的反应均完全进行)
②将少量二氧化碳通入大量澄清石灰水中,出现白色浑浊,且溶液质量减小.试解释溶液质量减小的原因:因为反应后有碳酸钙白色沉淀产生.
③对于该实验方案设计还存在不完善之处,你的具体改进方案是在装置最后添加一个点燃的酒精灯.
分析 (1)根据实验要求来连接实验仪器,根据反应的原理来书写化学方程式,根据酸碱指示剂的变色情况来分析;
(2)根据质量守恒定律进行分析解答;根据二氧化碳和氢氧化钙溶液反应生成了碳酸钙沉淀的缘故;从避免一氧化碳被排放到空气中来分析.
解答 解:(1)①用固态的石灰石与液态的稀盐酸反应来制取二氧化碳,选择B来制取,用饱和的碳酸氢钠溶液来除去二氧化碳中的氯化氢气体,用浓硫酸对二氧化碳进行干燥,最后用向上排空气法来进行收集;故填:BDAG;
②石灰石的主要成分是碳酸钙,与稀盐酸反应生成氯化钙、水和二氧化碳,故填:CaCO3+2HCl=CaCl2+H2O+CO2↑;
③二氧化碳与水反应生成碳酸,碳酸不能使无色酚酞试液变色,故填:无;
(2)①一氧化碳还原铁的氧化物,生成铁和二氧化碳,E处减少的质量即为铁的氧化物中氧元素的质量bg,则其中铁元素的质量为(a-b)g.
那么:$\frac{56x}{16y}=\frac{(a-b)g}{bg}$
$\frac{x}{y}=\frac{2(a-b)}{7a}$
故填:$\frac{2(a-b)}{7a}$;
②二氧化碳与氢氧化钙溶液反应生成了碳酸钙沉淀和水,故反应后溶液的质量减少了;故填:因为反应后有碳酸钙白色沉淀产生;
③尾气中含有的一氧化碳有毒,直接排放到空气中会造成空气污染,故填:在装置最后添加一个点燃的酒精灯.
点评 本考点主要考查了仪器的连接和气体的除杂和干燥,同时也考查了化学方程式的书写,综合性比较强,本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
相关题目
5.石油通过炼制得不到下列物质中的( )
| A. | 煤油 | B. | 液化石油气 | C. | 煤焦油 | D. | 汽油 |
2.下列安徽传统手工艺品的制作过程中,涉及化学变化的是( )
| A. |  阜阳剪纸 | B. |  徽州石刻 | C. |  舒席编织 | D. |  界首彩陶 |
5.对有关实验现象的描述正确的是( )
| A. | 碳在氧气中燃烧放出白烟 | |
| B. | 硫在氧气中燃烧产生淡蓝色的火焰 | |
| C. | 铁丝在氧气中燃烧生成黑色的四氧化三铁 | |
| D. | 一氧化碳在空气中燃烧产生蓝色火焰 |