题目内容
1.水煤气主要成分是一氧化碳、氢气及少量的二氧化碳和水蒸气.某兴趣小组同学为验证水煤气的成分.设计实验与装置如图所示: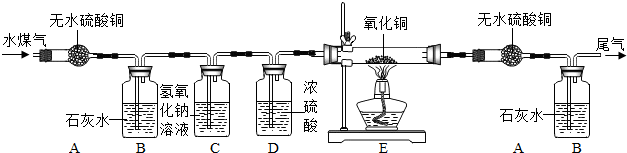
请分析上面信息后回答:
(1)你认为验证水煤气中各成分的顺序依次是H2O、CO2、H2、CO.
(2)装置D的作用是吸收水蒸气.
(3)装置E内观察到的现象是黑色固体逐渐变成红色.
(4〕实验中两次用到装置A,其目的分别是第一次使用装置A目的是验证水煤气中水蒸气的存在;第二次使用装置A目的是检验水煤气中是否含有氢气.
(5)请你设计一种尾气处理方案:将玻璃管改成尖嘴点燃或用气球收集.
分析 (1)根据水能使白色硫酸铜变蓝,二氧化碳能使澄清石灰水变浑浊,氢气还原氧化铜能生成水,一氧化碳还原氧化铜生成二氧化碳考虑本题;
(2)根据浓硫酸具有吸水性解答;
(3)根据氧化铜被还原成铜考虑实验现象解答;
(4)根据无水硫酸铜和水反应变蓝色考虑本题;
(5)一氧化碳是一种有毒的气体,尾气一般要收集火、点燃.
解答 解:(1)水能使白色硫酸铜变蓝,先通过无水硫酸铜是检验是否含有水的;二氧化碳能使澄清石灰水变浑浊,再通过石灰水是检验是否含有二氧化碳的;再通过氢氧化钠是除去原来的二氧化碳气体,通过浓硫酸是除去原来的水蒸气,通过氧化铜是检验是否含有还原性气体,再通过无水硫酸铜,是看是否有水生成,因为氢气还原氧化铜生成铜和水,所以是为了检验是否有氢气的;最后通过澄清石灰水是看有没有二氧化碳生成,由于一氧化碳还原氧化铜生成铜和二氧化碳,所以是为了检验是否含有一氧化碳的;
(2)浓硫酸具有吸水性,装置D的作用是吸收水蒸气
(3)氧化铜被还原成铜所以现象是黑色粉末变为红色;
(4)前面的装置A是为了检验是否有水生成,后面的装置A是为了检验是否有水生成,从而确定是否有氢气存在;
(5)尾气中含有一氧化碳,必须进行处理,方法是将玻璃管改成尖嘴点燃或用气球收集.
故答案为:(1)H2O、CO2、H2、CO;(2)吸收水蒸气;(3)黑色固体逐渐变成红色;(4)第一次使用装置A目的是验证水煤气中水蒸气的存在;第二次使用装置A目的是检验水煤气中是否含有氢气;(5)将玻璃管改成尖嘴点燃或用气球收集.
点评 本题以实验探究的形式考查常见气体氢气、一氧化碳、二氧化碳和水蒸气的性质,同学们要具有综合的化学知识才能做好此题.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
11.除去下列物质中的少量杂质,所选用的试剂和方法都正确的是( )
| 选项 | 物质 | 杂质 | 试剂、方法 |
| A | FeCl2(溶液) | CuCl2(溶液) | 铁粉、过滤 |
| B | CO2(气体) | HCl (气体) | 氢氧化钠溶液 |
| C | NaCl (溶液) | Na2CO3(溶液) | 稀硫酸 |
| D | KCl(固体) | MnO2 (固体) | 水、过滤 |
| A. | A | B. | B | C. | C | D. | D |
16.下列实验操作中,正确的是( )
| A. | 排水法收集氧气时,当导管口开始有气泡冒出时立即收集 | |
| B. | 稀释浓硫酸时,将浓硫酸沿烧杯壁缓缓注入盛有水的饶杯中,并用玻璃棒不断搅拌 | |
| C. | 过滤时,用玻璃棒在过滤器中不断搅拌 | |
| D. | 氢气、甲烷等可燃性气体点燃前进行验纯 |
13.在下列各种情况下,埋在地下的铸铁管道被腐蚀速率最慢的是( )
| A. | 在含砂粒较多、潮湿、透气的土壤中 | B. | 在干燥、致密、透气的土壤中 | ||
| C. | 在潮湿、疏松、透气的土壤中 | D. | 在呈酸性的潮湿土壤中 |
11. 下列各组物质中,存在如图所示的相互反应和转化关系的是( )
下列各组物质中,存在如图所示的相互反应和转化关系的是( )
 下列各组物质中,存在如图所示的相互反应和转化关系的是( )
下列各组物质中,存在如图所示的相互反应和转化关系的是( )| 选项 | 甲 | 乙 | 丙 | 丁 |
| A | O2 | CH4 | H2O | CO2 |
| B | C | Fe2O3 | Fe | CO2 |
| C | CuO | HCl | CuCl2 | H2O |
| D | CO2 | CaCl2 | CaCO3 | H2O |
| A. | A | B. | B | C. | C | D. | D |
 化学就在我们身边.
化学就在我们身边.
 如图所示是冶铁的反应原理,写出一氧化碳与氧化铁反应的现象固体由红棕色变化为黑色,反应方程式是Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,图中右边酒精的作用是点燃没有参与反应的CO.
如图所示是冶铁的反应原理,写出一氧化碳与氧化铁反应的现象固体由红棕色变化为黑色,反应方程式是Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,图中右边酒精的作用是点燃没有参与反应的CO.