题目内容
11.向装有等量水的A、B、C烧杯中分别加入10g、25g、25gNaNO3固体,充分溶解后,现象如图一所示.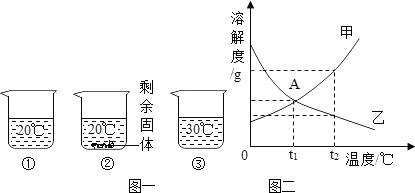
(1)烧杯中的溶液一定属于饱和溶液的是B(填序号);
(2)请写出图二中A 点的表示意义t1℃时,甲、乙两物质的溶解度相等;图二能表示NaNO3溶解度曲线的是甲(填“甲”或“乙”);
(3)由图二分析,若分别将100g甲、乙的饱和溶液从t2℃降温到t1℃,对所得溶液的叙述正确的BC(填序号,可多选).
A.甲、乙都是饱和溶液 B.溶剂质量:甲<乙 C.溶质质量分数:甲>乙
(4)欲除去混在甲中的少量乙物质可采用的方法是降温结晶(填“降温结晶”或“蒸发结晶”).
分析 根据溶液中是否有未溶解的溶质存在来判断溶液是否饱和,根据硝酸钠的溶解度随温度的变化确定硝酸钠的溶解度曲线;根据两种物质的溶解度曲线首先确定出在t2℃时两种物质的溶解度,从而可以确定出在t2℃时两种物质的饱和溶液中溶质的质量分数,及比较溶液中溶剂的多少;然后根据两种物质的溶解度随温度变化的情况,分析出降温至t1℃时两种物质的溶解度的大小,溶液状态的变化及溶液中各个量的变化.
解答 解:(1)由于在三个烧杯中只有B有未溶解的固体存在,因此B中的溶液一定是饱和溶液,故答案为:B
(2)由溶解度曲线可以看出甲乙物质的溶解度关系,t1℃时是甲乙二物质溶解度曲线的交点,即此温度时二者溶解度相等,故答案为:t1℃时,甲、乙两物质的溶解度相等;
由于在等量的30℃的水中全部溶解了25g硝酸钠,而20℃的水没有全部溶解25g硝酸钠,说明硝酸钠的溶解度随温度的升高而增大,故答案为:甲
(3)A、由于甲的溶解度随温度的降低而减小,因此它的饱和溶液降温后会有晶体析出,但溶液仍为饱和溶液;但乙的溶解度随温度的降低而增大,因此它的饱和溶液降温后就会变成不饱和溶液,故A错误;
B、由于在降温过程中溶剂的质量并没有发生变化,因此只要比较出它们原来的溶剂的多少即可;根据两种物质的溶解度曲线可知,在t2℃时,甲的溶解度大于乙的溶解度,即饱和溶液中溶质的质量分数甲>乙,即等量的饱和溶液中溶质的质量甲>乙,则溶剂甲<乙,故B正确;
C、在t1℃时,两物质的溶解度相等,即两物质的饱和溶液中溶质的质量分数相等,但乙溶液已经不再是饱和溶液,因此溶液中溶质的质量分数甲>乙,故C正确;
故选BC;
(4)甲的溶解度随温度的升高而增大,当甲中含有少量的乙时,采用降温结晶的方法,故答案为:降温结晶.
点评 本题难度较大,主要考查了固体溶解度曲线所表示的意义,及根据固体的溶解度曲线解决相关的问题,从而加深学生对固体溶解度的理解和掌握.

 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案| A. | 钛合金与人体有很好的“相容性”,可以用来制造人造骨 | |
| B. | 高炉炼铁是在高温下,利用炉内反应生成的一氧化碳把铁从铁矿石里还原出来炼得生铁 | |
| C. | 合金的熔点和硬度一般高于组成它们的纯金属,抗腐蚀性能也更好 | |
| D. | 日常生活中,大量使用的常常不是纯金属,而是它们的合金 |
 如图是a、b两种物质的溶解度曲线,下列分析正确的是( )
如图是a、b两种物质的溶解度曲线,下列分析正确的是( )| A. | 溶解度:a>b | |
| B. | 可采用降温方法将a的接近饱和的溶液变为饱和溶液 | |
| C. | 将t2℃时100ga的饱和溶液降温至t1℃,析出30ga | |
| D. | 将t2℃时a、b的饱和溶液降温至t1℃,所得溶液的溶质质量分数关系是a>b |
| 物质 |  |  |  |
| 化学式 | NaCl | Na2CO3 | (3)CaO |
| 用途 | (1)常用的调味品 | (2)用作面碱 | 做干燥剂 |




 ”、“○”、“●”代表不同原子,产物D为次氯酸(HClO),有杀菌消毒作用.
”、“○”、“●”代表不同原子,产物D为次氯酸(HClO),有杀菌消毒作用.