题目内容
16.某厂生产的产品碳酸钠中混有少量碳酸氢钠.为了测定产品中碳酸氢钠的质量分数,取100g样品加热(2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,碳酸钠受热不分解),完全分解生成二氧化碳气体0.22g.求样品中碳酸氢钠的质量分数.分析 根据碳酸氢钠受热分解的化学方程式,由产生二氧化碳的质量计算分解的碳酸氢钠的质量;进一步求样品中碳酸氢钠的质量分数.
解答 解:(1)解:设样品中碳酸氢钠的质量为X.
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑
168 44
X 0.22g
$\frac{168}{X}=\frac{44}{0.22g}$
X=0.84g
样品中碳酸氢钠的质量分数$\frac{0.84g}{100g}$×100%=0.84%.
答:样品中碳酸氢钠的质量分数为0.84%.
点评 此题是对化学方程式计算的考查,解题的关键是找到已知量,此题则是利用反应生成二氧化碳的质量求出其它物质的质量.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
7.如图是某化学反应的微观示意图,你认为下列说法不正确的是( )
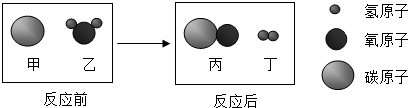

| A. | 反应前后原子的种类、数目都不变 | |
| B. | 该反应是置换反应 | |
| C. | 反应前后各元素的化合价都发生了改变 | |
| D. | 乙、丙两种物质都是氧化物 |
1.下列物质在氧气中燃烧现象描述正确的是( )
| A. | 木炭,白色火焰 | B. | 硫粉,淡蓝色火焰 | C. | 红磷,大量烟雾 | D. | 铁丝,火星四射 |
5.下列鉴别物质的方法错误的是( )
| A. | 用酚酞溶液鉴别氢氧化钠和碳酸钠 | |
| B. | 用水鉴别氢氧化钠和硝酸铵 | |
| C. | 用二氧化锰鉴别水和5%的过氧化氢溶液 | |
| D. | 用硝酸钡溶液鉴别稀盐酸和稀硫酸 |
6.用分子的知识解释生活中的现象,其中合理的是( )
| A. | 八月桂花飘香说明分子总是在不断运动 | |
| B. | 水结成冰,是因为温度降低,分子停止运动 | |
| C. | 酒精挥发说明酒精分子的体积增大 | |
| D. | 碳单质在不同条件下燃烧可生成一氧化碳,也可生成二氧化碳,说明同种分子化学性质不同 |