题目内容
17.请根据如图所示的实验过程和提供的数据计算
(1)合金中铜的质量分数是35%;
(2)所用稀硫酸的溶质质量分数是多少?(4分,写出计算过程,计算结果保留到0.1%)
分析 铜不能和稀硫酸反应,锌能和稀硫酸反应生成硫酸锌和氢气,最后所得溶液是硫酸锌溶液,根据硫酸锌溶液的质量、溶质质量分数可以计算反应生成氢气的质量、锌的质量、硫酸的质量,进一步可以计算合金中铜的质量分数和所用稀硫酸的溶质质量分数.
解答 解:(1)设锌的质量为x,硫酸的质量为y,反应生成氢气的质量为z
Zn+H2SO4═ZnSO4 +H2↑,
65 98 161 2
x y 100g×16.1% z
$\frac{65}{x}=\frac{98}{y}=\frac{161}{100g×16.1%}$
x=6.5g
y=9.8g
$\frac{161}{100g×16.1%}=\frac{2}{z}$
x=0.2g
合金中铜的质量分数为$\frac{10g-6.5g}{10g}$×100%=35%,
(2)设稀硫酸的质量为m,
6.5g+m-0.2g=100g,
m=93.7g,
所用稀硫酸的溶质质量分数为$\frac{9.8g}{93.7g}$×100%=10.5%,
答案:
(1)35%;
(2)所用稀硫酸的溶质质量分数为10.5%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.下列有关“守恒”的叙述中,正确的是( )
| A. | 镁带在空气中燃烧后,生成物的质量跟原镁带的质量相等 | |
| B. | 在反应3Cu+8HNO3═3Cu(NO3)2+2X↑+4H2O中的X的化学式是NO2 | |
| C. | 加热15.8gKMnO4,充分反应后,剩余固体的质量变为14.2g,则生成氧气1.6g | |
| D. | 某可燃物燃烧后生成的产物中有CO2、CO和SO2,则该物质一定含有碳、硫、氧元素 |
8.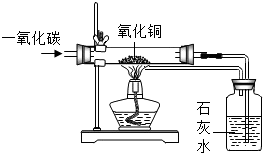 符合如图所示装置的选项是( )
符合如图所示装置的选项是( )
①说明一氧化碳具有还原性
②说明一氧化碳氧化后的产物是二氧化碳
③有效地防止了一氧化碳对空气的污染
④既能说明一氧化碳具有可燃性,又充分地利用了能源.
 符合如图所示装置的选项是( )
符合如图所示装置的选项是( )①说明一氧化碳具有还原性
②说明一氧化碳氧化后的产物是二氧化碳
③有效地防止了一氧化碳对空气的污染
④既能说明一氧化碳具有可燃性,又充分地利用了能源.
| A. | ①② | B. | ①②③ | C. | ②③④ | D. | 全部 |
2. 某同学为了进一步加深对“碱的化学性质”的理解,特邀你协助完成下列活动与探究:
某同学为了进一步加深对“碱的化学性质”的理解,特邀你协助完成下列活动与探究:
(1)如图所示,在白色点滴板上进行实验,请将实验现象填入下表:
(2)氢氧化钠溶液露置于空气中容易变质,请写出相关反应的化学方程式:2NaOH+CO2=Na2CO3+H2O.
(3)化学课后,化学兴趣小组的同学在整理实验桌时,发现有一瓶氢氧化钠溶液没有塞橡皮塞,征得老师同意后,开展了以下探究:
【猜想与假设】猜想1:部分变质. 猜想2:全部变质. 猜想3:没有变质.
【查阅资料】(1)氯化钙溶液呈中性.
(2)氯化钙溶液能与碳酸钠溶液反应:CaCl2+Na2CO3=CaCO3↓+2NaCl
【实验探究】
【实验结论】该氢氧化钠溶液部分(填“部分”或“全部”)变质.
【反思与评价】在上述实验探究中,小明提出可用氢氧化钙溶液代替氯化钙溶液,你认为该方案不可行(填“可行”或“不可行”).
 某同学为了进一步加深对“碱的化学性质”的理解,特邀你协助完成下列活动与探究:
某同学为了进一步加深对“碱的化学性质”的理解,特邀你协助完成下列活动与探究:(1)如图所示,在白色点滴板上进行实验,请将实验现象填入下表:
| 氢氧化钠溶液 | 氢氧化钙溶液 | |
| 加紫色石蕊溶液 | 溶液都变蓝色 | |
(3)化学课后,化学兴趣小组的同学在整理实验桌时,发现有一瓶氢氧化钠溶液没有塞橡皮塞,征得老师同意后,开展了以下探究:
【猜想与假设】猜想1:部分变质. 猜想2:全部变质. 猜想3:没有变质.
【查阅资料】(1)氯化钙溶液呈中性.
(2)氯化钙溶液能与碳酸钠溶液反应:CaCl2+Na2CO3=CaCO3↓+2NaCl
【实验探究】
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取少量该溶液于试管中,向溶液中滴加过量的氯化钙溶液,并不断振荡. | 有白色沉淀生成. | 说明原溶液中一定有碳酸钠. |
| (2)取步骤(1)试管中的少量上层清液,滴加酚酞溶液. | 溶液变红色. | 说明原溶液中一定有NaOH(氢氧化钠). |
【反思与评价】在上述实验探究中,小明提出可用氢氧化钙溶液代替氯化钙溶液,你认为该方案不可行(填“可行”或“不可行”).
19.下列实验操作不正确的是( )
| A. |  检查气密性 | B. |  验纯氢气 | C. |  检验氧气 | D. |  验满CO2 |