题目内容
5.化学材料和化学技术在智能房屋建设和家居生活中有着广泛的应用.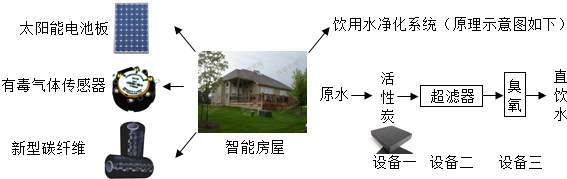
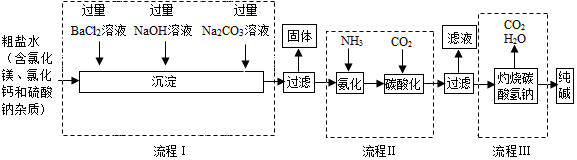
(1)智能房屋采用太阳能电池供电.生产太阳能电池需用纯硅.工业上由粗硅生产纯硅的工艺流程如图所示:

①上述步骤中属于物理变化的是步骤Ⅱ;
②写出步骤Ⅲ对应的化学方程式:SiCl4+2H2$\frac{\underline{\;110℃\;}}{\;}$Si+4HCl;
③与太阳能电池能量转化不同,火力发电是将化石燃料燃烧产生的热能转化为电能.
(2)有毒气体传感器可检测家用燃气不完全燃烧产生的有毒气体CO(填化学式),并及时报警.
(3)新型碳纤维密度比铝小,强度是铁的20倍,具有抗电磁辐射、耐腐蚀的特点,化学性质与碳相似.新型碳纤维在智能房屋建设中可用作AB(填下列选项字母).
A.建筑材料 B.电磁辐射屏蔽材料 C.防火材料
(4)饮用水净化系统中设备一和设备三的作用分别是吸附性、消毒.
分析 (1)①根据物理变化的定义进行分析;
②根据四氯化硅和氢气在加热的条件下反应生成硅和氯化氢进行分析;
③根据化石燃料燃烧会产生热量,所以火力发电是将化石燃料燃烧产生的热能转化为电能进行分析;
(2)根据含碳化合物不完全燃烧会产生一氧化碳进行分析;
(3)根据碳纤维的性质进行分析;
(4)根据活性炭具有吸附性,臭氧可以消毒进行分析.
解答 解:(1)①物理变化是没有新物质生成的变化,所以属于物理变化的是步骤Ⅱ;
②四氯化硅和氢气在加热的条件下反应生成硅和氯化氢,化学方程式为:SiCl4+2H2$\frac{\underline{\;110℃\;}}{\;}$Si+4HCl;
③化石燃料燃烧会产生热量,所以火力发电是将化石燃料燃烧产生的热能转化为电能;
(2)含碳化合物不完全燃烧会产生一氧化碳,一氧化碳有毒;
(3)碳纤维密度比铝小,强度是铁的20倍,具有抗电磁辐射、耐腐蚀的特点,化学性质与碳相似,所以新型碳纤维在智能房屋建设中可用作AB;
(4)活性炭具有吸附性,臭氧可以消毒.
故答案为:(1)①Ⅱ;②SiCl4+2H2$\frac{\underline{\;110℃\;}}{\;}$Si+4HCl;③热;
(2)CO;(3)AB;(4)吸附性,消毒.
点评 对知识进行迁移解决情形相似的新问题是本题的特点,体现出知识运用与问题分析的能力.

练习册系列答案
相关题目
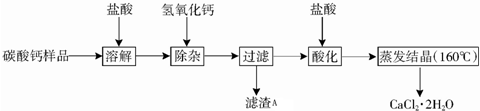
16.医用CaCl2•2H2O可用于补钙、抗过敏和消炎等,以某碳酸钙样品(其中含少量Al3+、Fe3+等杂质)生产医用CaCl2•2H2O的工艺流程为:
已知:查阅资料得知氢氧化物沉淀及溶解时的pH为:
(1)在实验室进行溶解时玻璃棒的作用是搅拌,加速溶解,过滤时用到的玻璃仪器有烧杯、玻璃棒、漏斗.
(2)除杂操作是加入稍过量的氢氧化钙,调节溶液的pH使Al3+、Fe3+全部转化为沉淀,此时应该控制溶液的pH值X的范围是4.0~7.8;滤渣A的主要成分的化学式为Fe(OH)3、Al(OH)3.
(3)酸化时加盐酸的主要目的为了将氢氧化钙转化为氯化钙.
(4)若所用碳酸钙样品12.5Kg,最后所得的产物中含氯化钙11.1Kg,则样品中碳酸钙的质量分数最大为多少?(写出计算过程)

已知:查阅资料得知氢氧化物沉淀及溶解时的pH为:
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Ca(OH)2 |
| 开始沉淀时的pH | 2.3 | 4.0 | 7.8 |
| 完全沉淀时的pH | 3.7 | 5.2 | 10.8 |
(2)除杂操作是加入稍过量的氢氧化钙,调节溶液的pH使Al3+、Fe3+全部转化为沉淀,此时应该控制溶液的pH值X的范围是4.0~7.8;滤渣A的主要成分的化学式为Fe(OH)3、Al(OH)3.
(3)酸化时加盐酸的主要目的为了将氢氧化钙转化为氯化钙.
(4)若所用碳酸钙样品12.5Kg,最后所得的产物中含氯化钙11.1Kg,则样品中碳酸钙的质量分数最大为多少?(写出计算过程)
14.下列实验中不可能成功的是( )
| A. | 将一只冷碟子放在蜡烛火焰上方获得炭黑 | |
| B. | 用过滤法使硬水转化成软水 | |
| C. | 用食醋区分食盐和纯碱 | |
| D. | 用牵牛花和酒精自制酸碱指示剂 |
15. 以下关于氮元素的说法错误的是( )
以下关于氮元素的说法错误的是( )
 以下关于氮元素的说法错误的是( )
以下关于氮元素的说法错误的是( )| A. | 如图中的一条信息:氮元素相对原子质量为14.01 | |
| B. | NH4NO3中含有氮元素,可用作化学肥料 | |
| C. | 空气中含量最多的元素是氮元素 | |
| D. | KNO3中氮元素的化合价为+1 |