题目内容
元素周期表是学习和研究化学的重要工具,它的内容十分丰富.如表是元素周期表的部分内容,请认真分析并回答后面的问题:
(1)表中不同种元素最本质的区别是 (填序号):
A.相对原子质量不同 B.质子数不同 C.中子数不同 D.核外电子数
(2)生物体内含量最多的元素的符号是 ;
(3)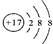 表示的是(填名称) ;
表示的是(填名称) ;
(4)由8、11号元素组成化合物的化学式 .
(5)地壳中含量最多的金属元素、非金属元素及空气中含量最多的元素形成化合物的化学式 .
(6)元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律,如: (填字母序号)
A.从左到右,各元素原子的电子层数相同
B.从左到右,各元素原子的原子序数依次增加
C.从左到右,各元素原子的最外层电子数相同
(7)元素周期表中,原子序数为12的镁元素的原子结构示意图如图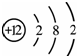 ,该原子在化学反应中易 (填“得到”或“失去”)电子,说明元素的化学性质与原子的 关系密切,镁元素在化合物中的化合价是 价,镁的氧化物的化学式是 .
,该原子在化学反应中易 (填“得到”或“失去”)电子,说明元素的化学性质与原子的 关系密切,镁元素在化合物中的化合价是 价,镁的氧化物的化学式是 .
| ⅠA | 0 | ||||||||
| 1 | 1 H 氢 1.008 |
2 He 氦 4.003 |
|||||||
| ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | ||||
| 2 | 3 Li 锂 6.941 |
4 Be 铍 9.012 |
5 B 硼 10.81 |
6 C 碳 12.01 |
7 N 氮 14.01 |
8 O 氧 16.00 |
9 F 氟 19.00 |
10 Ne 氖 20.18 |
|
| 3 | 11 Na 钠 22.99 |
12 Mg 镁 24.31 |
13 Al 铝 26.98 |
14 Si 硅 28.09 |
15 P 磷 30.97 |
16 S 硫 32.06 |
17 Cl 氯 35.45 |
18 Ar 氩 39.95 |
|
A.相对原子质量不同 B.质子数不同 C.中子数不同 D.核外电子数
(2)生物体内含量最多的元素的符号是
(3)
 表示的是(填名称)
表示的是(填名称)(4)由8、11号元素组成化合物的化学式
(5)地壳中含量最多的金属元素、非金属元素及空气中含量最多的元素形成化合物的化学式
(6)元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律,如:
A.从左到右,各元素原子的电子层数相同
B.从左到右,各元素原子的原子序数依次增加
C.从左到右,各元素原子的最外层电子数相同
(7)元素周期表中,原子序数为12的镁元素的原子结构示意图如图
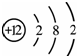 ,该原子在化学反应中易
,该原子在化学反应中易考点:元素周期表的特点及其应用,原子结构示意图与离子结构示意图,元素的概念,化学符号及其周围数字的意义
专题:化学用语和质量守恒定律
分析:(1)掌握元素的概念:具有相同核电荷数(核内质子数)的一类原子的总称;
(2)生物体中含量最多的元素是氧元素;
(3)根据质子数确定元素种类,根据质子数和核外电子数确定带电情况;
(4)根据原子序数确定元素种类,并书写化学式;
(5)根据我们教材中学习的知识可以回答此题.空气中含量最多的元素是氮元素;地壳中含量最多的非金属元素是氧;地壳中含量最多的金属元素是铝元素,然后确定化学式;
(6)总结归纳是学习化学的一种重要方法:元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律;
(7)依据其最外层电子数,推测其得失电子情况并进而发现元素的性质和最外层电子数的关系,推断出其化合价,并书写化学式.
(2)生物体中含量最多的元素是氧元素;
(3)根据质子数确定元素种类,根据质子数和核外电子数确定带电情况;
(4)根据原子序数确定元素种类,并书写化学式;
(5)根据我们教材中学习的知识可以回答此题.空气中含量最多的元素是氮元素;地壳中含量最多的非金属元素是氧;地壳中含量最多的金属元素是铝元素,然后确定化学式;
(6)总结归纳是学习化学的一种重要方法:元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律;
(7)依据其最外层电子数,推测其得失电子情况并进而发现元素的性质和最外层电子数的关系,推断出其化合价,并书写化学式.
解答:解:(1)根据元素的概念,可知表中不同种元素最本质的区别是质子数不同,故选B;
(2)生物体中含量最多的元素是氧元素,氧的元素符号是O;
(3)该粒子的核电荷数为17,核外有18个电子,带一个单位的负电荷,是氯离子;
(4)8号元素是氧元素,11号元素是钠元素,组成的化合物的化学式为Na2O;
(5)空气中含量最多的元素是氮元素;地壳中含量最多的非金属元素是氧;地壳中含量最多的金属元素是铝元素,这三种元素组成的化合物是硝酸铝;
(6)元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律:A.从左到右,各元素原子的电子层数相同;B.从左到右,各元素原子的原子序数依次增加;
(7)利用原子序数为12的镁元素的原子结构示意图,可知其最外层电子数是2,小于4在化学反应中易失去电子,说明元素的化学性质与原子的最外层电子数关系密切.镁原子易失去2个电子而显+2价,其氧化物的化学式为MgO.
故答案为:(1)B;(2)O;(3)氯离子;(4)Na2O;(5)Al(NO3)3;(6)AB;(7)失去;最外层电子数;+2;MgO.
(2)生物体中含量最多的元素是氧元素,氧的元素符号是O;
(3)该粒子的核电荷数为17,核外有18个电子,带一个单位的负电荷,是氯离子;
(4)8号元素是氧元素,11号元素是钠元素,组成的化合物的化学式为Na2O;
(5)空气中含量最多的元素是氮元素;地壳中含量最多的非金属元素是氧;地壳中含量最多的金属元素是铝元素,这三种元素组成的化合物是硝酸铝;
(6)元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律:A.从左到右,各元素原子的电子层数相同;B.从左到右,各元素原子的原子序数依次增加;
(7)利用原子序数为12的镁元素的原子结构示意图,可知其最外层电子数是2,小于4在化学反应中易失去电子,说明元素的化学性质与原子的最外层电子数关系密切.镁原子易失去2个电子而显+2价,其氧化物的化学式为MgO.
故答案为:(1)B;(2)O;(3)氯离子;(4)Na2O;(5)Al(NO3)3;(6)AB;(7)失去;最外层电子数;+2;MgO.
点评:了解元素周期表的特点及其应用;核外电子在化学反应中的作用;了解地壳中元素的分布与含量;了解原子结构示意图与离子结构示意图的特点.掌握原子结构相关知识的考查;掌握核外电子在化学反应中的作用;了解原子结构示意图的意义是解题的关键.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
 实验小组同学用CO与铁的氧化物反应利用如图的实验装置进行实验
实验小组同学用CO与铁的氧化物反应利用如图的实验装置进行实验 元素周期表是学习和研究化学的重要工具.如表是周期表的部分信息:
元素周期表是学习和研究化学的重要工具.如表是周期表的部分信息:

 实验室常用如图装置来制取氧气:
实验室常用如图装置来制取氧气: