题目内容
元素周期表是学习和研究化学的工具.下表是元素周期表的一部分.
(1)很多科学家对元素周期表的发现和完善做出了重大贡献,请写出其中一位科学家的名字:
(2)查出碳的原子序号: ,写出16号元素的元素符号 ,属于 元素(金属或非金属)
(3)表中不同种元素最本质的区别是 (填序号)
A质子数不同 B中子数不同 C相对原子质量不同 D电子数不同
(4)利用元素周期表,人们对元素的认识进入全新的飞跃时期.近日,俄罗斯科学家宣布他们将人工合成第118号元素,则此元素的核电荷数为 .
(5)根据第二周期我们可知周期表的排列规律 .
| 族/周期 | ⅠA |
0 | ||||||
| 1 | 1 H 氢 1.008 |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
2 He 氦 4.003 |
| 2 |
3 Li 锂 6.941 |
4 Be 铍 9.012 |
5 B 硼 10.81 |
6 C 碳 12.01 |
7 N 氮 14.01 |
8 O 氧 16.00 |
9 F 氟 19.00 |
10 Ne 氖 20.81 |
| 3 | 11 Na 钠 22.99 |
12 Mg 镁 24.31 |
13 Al 铝 26.98 |
14 Si 硅 28.09 |
15 P 磷 30.97 |
16 S 硫 32.06 |
17 Cl 氯 35.45 |
18 Ar 氩 39.95 |
(2)查出碳的原子序号:
(3)表中不同种元素最本质的区别是
A质子数不同 B中子数不同 C相对原子质量不同 D电子数不同
(4)利用元素周期表,人们对元素的认识进入全新的飞跃时期.近日,俄罗斯科学家宣布他们将人工合成第118号元素,则此元素的核电荷数为
(5)根据第二周期我们可知周期表的排列规律
考点:元素周期表的特点及其应用,元素的概念
专题:化学用语和质量守恒定律
分析:(1)可从门捷列夫发现并改进元素周期表填空;
(2)根据元素周期表中碳和硫元素的信息,即可查出其原子序数和元素符号,根据化学元素汉字名称的偏旁可辨别元素的种类;
(3)不同元素的区别是质子数不同;
(4)根据在原子中,原子序数=质子数=核电荷数=核外电子数,进行解答;
(3)依据同一周期的元素的共同点分析解答.
(2)根据元素周期表中碳和硫元素的信息,即可查出其原子序数和元素符号,根据化学元素汉字名称的偏旁可辨别元素的种类;
(3)不同元素的区别是质子数不同;
(4)根据在原子中,原子序数=质子数=核电荷数=核外电子数,进行解答;
(3)依据同一周期的元素的共同点分析解答.
解答:解:(1)科学家门捷列夫发现并完善了元素周期表,对元素周期表做出了巨大的贡献;
(2)由表中信息可知碳的原子序数是 12,16号元素是硫,元素符号:S,硫元素名称中偏旁是“石”,属于非金属元素.
(3)不同元素最本质的区别是核电荷数不同,也就是核内质子数不同.
(4)根据在原子中,原子序数=质子数=核电荷数=核外电子数,可知原子序数为118元素的核电荷数为:118;
(5)根据元素周期表的部分信息可知元素周期表同一横行元素的排列规律是:从左至右金属元素→非金属元素→稀有气体元素,原子序数(核电荷数)依次增大等.
故答案为:(1)门捷列夫;
(2)12;S;非金属;
(3)A;
(4)118;
(5)原子序数(核电荷数)依次增大.
(2)由表中信息可知碳的原子序数是 12,16号元素是硫,元素符号:S,硫元素名称中偏旁是“石”,属于非金属元素.
(3)不同元素最本质的区别是核电荷数不同,也就是核内质子数不同.
(4)根据在原子中,原子序数=质子数=核电荷数=核外电子数,可知原子序数为118元素的核电荷数为:118;
(5)根据元素周期表的部分信息可知元素周期表同一横行元素的排列规律是:从左至右金属元素→非金属元素→稀有气体元素,原子序数(核电荷数)依次增大等.
故答案为:(1)门捷列夫;
(2)12;S;非金属;
(3)A;
(4)118;
(5)原子序数(核电荷数)依次增大.
点评:本题难度不大,考查学生灵活运用元素周期表中元素的信息等进行分析解题的能力.注意:原子序数=质子数=核电荷数=核外电子数的前提条件是:在原子中.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 用如图装置进行实验时.观察到下层蜡烛比上层蜡烛先熄灭,由此不能得出的实验结论是( )
用如图装置进行实验时.观察到下层蜡烛比上层蜡烛先熄灭,由此不能得出的实验结论是( )| A、二氧化碳不能燃烧 |
| B、二氧化碳不能支持燃烧 |
| C、二氧化碳的密度比空气的大 |
| D、二氧化碳能溶于水 |
A、B、C、D四种短周期元素的原子半径次减小,A与C的核电荷数之比为3:4,D分别能与A、B、C形成电子总数相等的分子X、Y、Z.下列叙述不正确的是( )
| A、X、Y、Z的稳定性逐渐减弱 |
| B、A、D能形成多种化合物 |
| C、C、D组成的某种化合物在常温下呈液态 |
| D、X、Y、Z三种化合物的熔、沸点逐渐升高 |
物质的用途错误的是( )
| A、氯化钠可用作干燥剂 |
| B、金刚石用于切割玻璃 |
| C、稀有气体用于制作霓虹灯 |
| D、干冰用于人工降雨 |
小明奶奶为他迎接中考制定了如下食谱:米饭、红绕鸡、糖醋鱼、麻辣豆腐、蛋汤.为使营养均衡,你觉得还要补充( )
| A、牛肉 | B、青菜 | C、河虾 | D、水果 |
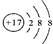 表示的是(填名称)
表示的是(填名称)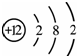 ,该原子在化学反应中易
,该原子在化学反应中易