题目内容
向50g 0.8%的氢氧化钠溶液中加入一定量的稀硫酸恰好完全反应,此时,溶液pH=7.
(1)求反应前氢氧化钠溶液中溶质的质量;
(2)求参加反应的硫酸的质量;
(3)求反应后,生成硫酸钠的质量.
解:(1)氢氧化钠的质量=50.0g×8.0%=4.0g
(2)设参加反应的硫酸的质量为y,反应后溶液中硫酸钠的质量为x.
H2SO4+2NaOH=Na2SO4+2H2O
98 80 142
y 4.0g x
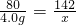
x=7.1g
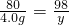
y=4.9g
答:(1)反应前氢氧化钠溶液中溶质的质量为4.0g;
(2)参加反应的硫酸的质量4.9g;
(3)反应后,生成硫酸钠的质量为7.1g.
分析:根据“溶液质量×溶质质量分数=溶液中溶质的质量”就可计算出反应前氢氧化钠溶液中溶质的质量;根据氢氧化钠与硫酸反应的化学方程式和参与反应的NaOH的质量,列出比例式,就可计算出参加反应的硫酸的质量以及反应后生成硫酸钠的质量.
点评:本题主要考查学生运用化学方程式和溶质质量分数公式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.
(2)设参加反应的硫酸的质量为y,反应后溶液中硫酸钠的质量为x.
H2SO4+2NaOH=Na2SO4+2H2O
98 80 142
y 4.0g x
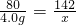
x=7.1g
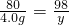
y=4.9g
答:(1)反应前氢氧化钠溶液中溶质的质量为4.0g;
(2)参加反应的硫酸的质量4.9g;
(3)反应后,生成硫酸钠的质量为7.1g.
分析:根据“溶液质量×溶质质量分数=溶液中溶质的质量”就可计算出反应前氢氧化钠溶液中溶质的质量;根据氢氧化钠与硫酸反应的化学方程式和参与反应的NaOH的质量,列出比例式,就可计算出参加反应的硫酸的质量以及反应后生成硫酸钠的质量.
点评:本题主要考查学生运用化学方程式和溶质质量分数公式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目
下表列出了NH4Cl在不同温度下的溶解度:
(1)10℃时,将20g NH4Cl加入到100g水中,充分搅拌,形成的溶液属于 (填“饱和”或“不饱和”)溶液,该溶液的溶质质量分数为 .
(2)20℃时,向50g水中加入20g NH4Cl,充分搅拌,NH4Cl未能全部溶解,此时该溶液中溶质与溶剂的质量比为 ;要使NH4Cl全部溶解,你的方法是 、 (写出两种方法).
(3)由上表可推出溶解度曲线的变化规律是 .
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 溶解度/g | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | 60.2 | 65.6 |
(2)20℃时,向50g水中加入20g NH4Cl,充分搅拌,NH4Cl未能全部溶解,此时该溶液中溶质与溶剂的质量比为
(3)由上表可推出溶解度曲线的变化规律是