题目内容
1.根据下列装置,结合所学化学知识回答下列问题.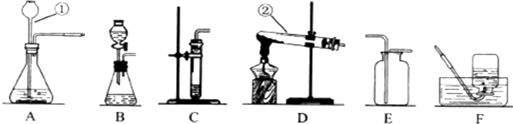
(1)请写出图中标号仪器的名称:①长颈漏斗;②试管.
(2)实验室用过氧化氢溶液制取氧气时,发生装置最好选用A或B,收集装置选用E或F,该反应的符号表达式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
如需随时控制生产气体的量并节约药品,发生装置最好选用B(填编号)
(3)实验室用氯酸钾制取氧气时,发生装置应选用D(填编号);写出其反应的符号表达式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(4)用F装置收集一瓶O2做铁丝燃烧实验:
判断铁丝在氧气中燃烧是化学变化的主要依据是B
A.发生白光 B.生成黑色固体 C.放热 D.剧烈燃烧,火星四射
该反应的符号表达式3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;集气瓶底要预先留少量的水会铺一层细沙,目的是防止铁的熔化物溅落.
(5)用装置D制取氧气时,试管口略向下倾斜的原因是防止水倒流而炸裂试管.
(6)实验室里用加热高锰酸钾的方法制取氧气,并用排水法收集氧气实验时,待气泡放出时,不宜立即收集,其原因是装置内有空气;应待气泡均匀、连续冒出时,再收集.实验结束时应先把导管移出水槽,后熄灭酒精灯,原因是防止水倒流而炸裂试管;集满氧气的集气瓶应正放在桌上并盖上玻璃片.
分析 长颈漏斗方便加液体药品,试管是常用的反应容器;制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.判断铁丝在氧气中燃烧是化学变化的主要依据是:生成黑色固体,即有新物质生成;铁和氧气在点燃的条件下生成四氧化三铁,配平即可,集气瓶底要预先留少量的水会铺一层细沙,目的是防止铁的熔化物溅落,而炸裂集气瓶;用装置D制取氧气时,试管口略向下倾斜的原因是:防止水倒流而炸裂试管;实验室里用加热高锰酸钾的方法制取氧气,并用排水法收集氧气实验时,待气泡放出时,不宜立即收集,其原因是装置内有空气,应待气泡均匀、连续冒出时,再收集;实验结束应先移出导管,后熄灭酒精灯,其原因是:防止水倒流,使试管炸裂.用排水法收集较纯净氧气的适宜时间是:当导管口有连续均匀气泡冒出时;集满氧气的集气瓶应正放在桌上并盖上玻璃片.
解答 解:(1)长颈漏斗方便加液体药品,试管是常用的反应容器,故答案为:长颈漏斗;试管;
(2)如果用双氧水和二氧化锰制氧气就不需要加热,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;分液漏斗可以控制反应的速度;故答案为:A或B;E或F;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;B;
(3)如果用氯酸钾制氧气就需要加热,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,配平即可;故答案为:D;2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(4)判断铁丝在氧气中燃烧是化学变化的主要依据是:生成黑色固体,即有新物质生成;铁和氧气在点燃的条件下生成四氧化三铁,配平即可,集气瓶底要预先留少量的水会铺一层细沙,目的是防止铁的熔化物溅落,而炸裂集气瓶;故答案为:B;3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;留少量的水会铺一层细沙,目的是防止铁的熔化物溅落;
(5)用装置D制取氧气时,试管口略向下倾斜的原因是:防止水倒流而炸裂试管;故答案为:防止水倒流而炸裂试管;
(6)实验室里用加热高锰酸钾的方法制取氧气,并用排水法收集氧气实验时,待气泡放出时,不宜立即收集,其原因是装置内有空气,应待气泡均匀、连续冒出时,再收集;实验结束应先移出导管,后熄灭酒精灯,其原因是:防止水倒流,使试管炸裂.用排水法收集较纯净氧气的适宜时间是:当导管口有连续均匀气泡冒出时;集满氧气的集气瓶应正放在桌上并盖上玻璃片;故答案为:装置内有空气;气泡均匀、连续冒出;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和氧气的性质等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

| 叙述Ⅰ | 叙述Ⅱ | |
| A | 二氧化碳能与水反应生成碳酸 | 正常雨水显酸性,称为酸雨 |
| B | 电解水生成氢气和氧气 | 水由氢元素和氧元素组成 |
| C | 分子在不断的运动 | 5mL水和5mL酒精混合后小于10mL |
| D | 酸可与碱发生中和反应 | 用氢氧化钠改良酸性土壤 |
| A. | A | B. | B | C. | C | D. | D |
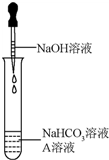 同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?
同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.
(1)实验准备
①查阅资料:NaHCO3+NaOH═Na2CO3+H2O
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$NaCO3+H2O+CO2↑
②用一定溶质的质量分数的NaHCO3、NaOH和Na2CO3三种溶液进行如下实验,为设计实验方案提供参考.
| NaHCO3溶液 | NaOH溶液 | Na2CO3溶液 | |
| 加入稀盐酸 | Ⅰ | 无明显变化 | 产生气泡 |
| 加入澄清石灰水 | 溶液变浑浊 | 无明显变化 | Ⅱ |
| 加入CaCl2溶液 | 无明显变化 | 溶液变浑浊 | 溶液变浑浊 |
| 加热溶液至沸腾,将 气体通入澄清石灰水 | 澄清石灰水 变浑浊 | 澄清石灰水 无明显变化 | 澄清石灰水 无明显变化 |
(2)实验过程:[实验1]证明反应生成了Na2CO3同学们选用上表实验中的药品,设计了如图所示实验,先在NaHCO3溶液中加入A溶液,无明显现象,再滴加NaOH溶液,溶液变浑浊,则A溶液是CaCl2. 有同学提出这个实验不足以证明有Na2CO3生成,其理由是_CaCl2 和NaOH反应生成Ca(OH)2,氢氧化钙是微溶物,在溶液中也产生沉淀.为了证明有Na2CO3生成,需要继续进行的操作是取少量反应后滤渣加入足量的稀盐酸,若产生无色气体证明有Na2CO3生成,反之则没有.
[实验2]证明反应后NaHCO3不存在
同学们参考上表中的实验,又设计了一个实验,虽然没有观察到明显的实验现象,但可以证明反应发生了,该实验方案是取少量反应后的溶液加热至沸腾,将气体通入澄清石灰水,若澄清石灰水变浑浊,证明有:NaHCO3存在,反之则没有.
(3)实验反思
通过实验1和实验2说明,对于没有明显现象的化学反应,可以从两个不同的角度证明反应的发生,这两个角度是一是可以通过检验反应物证明反应发生,二是可以通过检验产物证明反应发生.
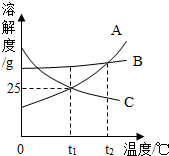 如图是A、B、C三种固体物质的溶解度曲线.下列说法正确的是( )
如图是A、B、C三种固体物质的溶解度曲线.下列说法正确的是( )| A. | t1℃时,A的饱和溶液中溶质质量分数为25% | |
| B. | t2℃时,A、B、C三种物质的溶解度大小关系为A=B>C | |
| C. | 将t1℃时A、C的饱和溶液升温到t2℃时,A、C两溶液都会变成不饱和溶液 | |
| D. | A中含有少量B,要提纯A通常可采用蒸发结晶的方法 |
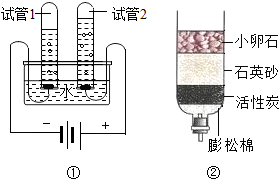 水是生命之源,人类的日常生活与工农业生产都离不开水.
水是生命之源,人类的日常生活与工农业生产都离不开水. 如图是a、b、c三种物质(均不含结晶水)的溶解度曲线,请你回答:
如图是a、b、c三种物质(均不含结晶水)的溶解度曲线,请你回答: “低碳生活,绿色出行”.如图为潍坊公共自行车.请回答下列问题:
“低碳生活,绿色出行”.如图为潍坊公共自行车.请回答下列问题: