题目内容
17.酸、碱、盐在生活、生产中应用广泛,为了便于理解和记忆,小丽同学总结了碱的化学性质如图,请你根据要求完成下列问题: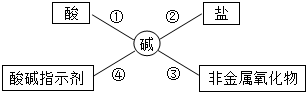
(1)小丽同学发现,以前取用氢氧化钠溶液时试剂瓶忘记盖瓶塞,依据反应③说明NaOH必须密封保存,否则在空气中要变质,如果该溶液变质,则发生反应的化学方程式为2NaOH+CO2═Na2CO3+H2O;
(2)要检验该氢氧化钠溶液已变质,选择下列试剂不能达到目的是B
A.稀HCl B.酚酞试液 C.CaCl2 D.Ca(OH)2
(3)依据反应②,KOH能与下列物质反应的是C
A.H2SO4 B.BaCl2 C.CuSO4 D.Na2CO3
(4)硫酸铵[(NH4)2SO4]、磷酸二氢钙[Ca(H2PO4)2]、亚硝酸钠(NaNO2)、硝酸钾(KNO3)等属于盐,其中又属于复合肥的是硝酸钾(KNO3).
分析 (1)根据氢氧化钠能够吸收空气中的二氧化碳,并且能够反应生成碳酸钠和水解答;
(2)根据氢氧化钠变质,氢氧化钠溶液中就含有碳酸钠,碳酸钠显碱性,只要能证明溶液中是否含有碳酸根离子就能判断氢氧化钠溶液是否变质;
(3)根据复分解反应发生的条件解答;
(4)根据复合肥是含有两种或两种以上营养元素的化肥解答.
解答 解:(1)氢氧化钠和二氧化碳发生反应生成碳酸钠和水,化学方程式为:2NaOH+CO2═Na2CO3+H2O,故填:2NaOH+CO2═Na2CO3+H2O;
(2)A、滴加盐酸,有气泡生成,说明溶液中含有碳酸钠,因此盐酸能验证氢氧化钠溶液已变质,故选项不符合题意;
B、氢氧化钠变质,氢氧化钠溶液中含有碳酸钠,碳酸钠也显碱性,也能使酚酞试液变红色,因此无色酚酞不能验证氢氧化钠溶液已变质,故选项符合题意;
C、滴加氯化钙溶液,有白色沉淀生成,说明溶液中含有碳酸钠,因此氯化钙溶液能验证氢氧化钠溶液已变质,故选项不符合题意;
D、滴加氢氧化钙溶液,有白色沉淀生成,说明溶液中含有碳酸钠,因此氢氧化钙溶液能验证氢氧化钠溶液已变质,故选项不符合题意.
故选:B;
(3)依据反应②,碱可以和盐反应.
A、H2SO4 是酸,故错误;
B、BaCl2是盐,和KOH相互交换成分没有气体、沉淀和水生成,不反应,故错误;
C、CuSO4 是盐,和KOH相互交换成分有氢氧化铜蓝色沉淀生成,反应,故正确;
D、Na2CO3是盐,和KOH相互交换成分没有气体、沉淀和水生成,不反应,故错误;
故选C;
(4)硫酸铵[(NH4)2SO4]属于氮肥,磷酸二氢钙[Ca(H2PO4)2]属于磷肥;亚硝酸钠(NaNO2)属于氮肥,硝酸钾(KNO3)中含有氮元素和钾元素,属于复合肥,故填:硝酸钾(KNO3).
点评 本题主要考查NaOH的化学性质和碳酸盐的检验,难度不大,是对所学知识的综合运用,需要学生具备扎实的基础知识与综合运用知识分析问题、解决问题的能力,学习中全面把握基础知识.

 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案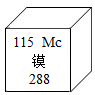 2017年5月,中国科学院,国家语言文字工作委员会,全国科学技术名词审定委员会在北京联合举行新闻发布会,正式向社会发布115号等元素的中文名称,115号元素的相关信息如图所示,有关该元素说法不正确的是( )
2017年5月,中国科学院,国家语言文字工作委员会,全国科学技术名词审定委员会在北京联合举行新闻发布会,正式向社会发布115号等元素的中文名称,115号元素的相关信息如图所示,有关该元素说法不正确的是( )| A. | 属于非金属元素 | B. | 原子序数为115 | C. | 元素名称为镆 | D. | 元素符号为Mc |
| 温度 | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度(g) | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
(2)温度为20℃时,在装有5g硝酸钾晶体的试管中,加入10g水并充分振荡,此时所得溶液为饱和(选填“饱和”或“不饱和”)溶液.再将该试管放入盛有热水的烧杯中,使试管内溶液温度升至60℃,此时试管内的溶液中溶质与溶剂的质量比为1:2.
(3)硝酸钾属于易溶(填“易溶”、“可溶”、“微溶”或“难溶”)物质.

| A. | t1℃时两种物质的饱和溶液中含有溶质的质量相等 | |
| B. | t2℃时a的溶解度大于b | |
| C. | t2℃时,a的不饱和溶液通过蒸发溶剂或增加a物质可变成饱和 | |
| D. | 当a中含有少量b时,可采用冷却热饱和溶液的方法提纯a |