题目内容
12.(1)根据质量守恒定律进行解释,细铁丝在氧气中燃烧,生成物的质量比细铁丝的质量大.(2)做铁丝和硫在氧气中燃烧实验时,集气瓶中都预先留少量水其目的分别是什么?
(3)氨气与酸反应可生成铵盐(白色固体).将分别蘸有浓氨水和浓盐酸的玻璃棒接近(不接触),就有大量白烟产生,请解释白烟产生的原因.
分析 (1)从质量守恒定律的定义来解答.参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和,质量守恒定律适合所有的化学反应,有些反应表面上不符合质量守恒,那是忽略了某些气体反应物或生成物的质量;
(2)考虑铁在氧气中燃烧能生成高温熔融物四氧化三铁,硫在氧气中燃烧能生成二氧化硫,二氧化硫是大气污染物;
(3)根据浓盐酸易挥发出的氯化氢气体能与氨气化合生成了氯化铵颗粒分析回答.
解答 解:(1)因为质量守恒定律适合所有的化学反应,铁丝在氧气中燃烧反应物是铁和氧气,生成的四氧化三铁的质量是铁和与它反应的氧气的质量的和,所以要比铁的质量大;
(2)做铁丝在氧气中燃烧实验中,集气瓶底部加有少量的水是防止溅落的熔融物炸裂瓶底;硫在氧气中燃烧生成的二氧化硫是一种大气污染物,能和水反应生成亚硫酸,所以硫在氧气中燃烧实验时,集气瓶底部加有少量的水目的是吸收有害气体,防止污染空气;
(3)浓盐酸易挥发出的氯化氢气体能与氨气化合生成了氯化铵颗粒,所以,将分别蘸有浓氨水和浓盐酸的玻璃棒接近(不接触),就有大量白烟产生.
故答案为:
(1)参加反应的铁和氧气的质量总和等于生成的四氧化三铁的质量;
(2)防止溅落的熔融物炸裂瓶底;吸收二氧化硫防止污染空气;
(3)浓盐酸易挥发出氯化氢气体,氯化氢气体能与氨气化合生成了氯化铵颗粒.
点评 本题考查了铁丝、硫粉与氧气反应的实验注意事项,要明确这两个实验相同点都是集气瓶中放了水,但是它们的目的不同.

练习册系列答案
相关题目
2.下列说法中,错误的是( )
| A. | 少量有害气体进入空气中,依靠大自然的自净能力,空气仍能保持洁净 | |
| B. | 空气中的O2只有点燃时才能发生化学反应 | |
| C. | 氮气充入食品包装袋内可以防腐 | |
| D. | 稀有气体充入灯泡中可使其耐用 |
7.根据化学方程式A+NaOH═B+H2O推断,B、A的相对分子质量相差为( )
| A. | 22 | B. | 40 | C. | 12 | D. | 18 |
17.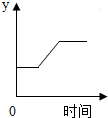 已知在实验室中用加热高锰酸钾的方法来制取氧气,如图表示一定质量的高锰酸钾受热过程中,某变量y随时间的变化趋势,纵坐标表示的是( )
已知在实验室中用加热高锰酸钾的方法来制取氧气,如图表示一定质量的高锰酸钾受热过程中,某变量y随时间的变化趋势,纵坐标表示的是( )
 已知在实验室中用加热高锰酸钾的方法来制取氧气,如图表示一定质量的高锰酸钾受热过程中,某变量y随时间的变化趋势,纵坐标表示的是( )
已知在实验室中用加热高锰酸钾的方法来制取氧气,如图表示一定质量的高锰酸钾受热过程中,某变量y随时间的变化趋势,纵坐标表示的是( )| A. | 固体中氧元素的质量 | B. | 生成氧气的质量 | ||
| C. | 生成二氧化锰的质量 | D. | 固体中钾元素的质量分数 |
4.下列物质的用途中,利用其物理性质的是( )
| A. | 氧气用于炼钢 | B. | 天然气用作燃料 | ||
| C. | 氦气用于充灌气球 | D. | 氮气用于食品包装的保护气 |
