题目内容
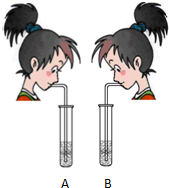 化学课上,老师展示了A、B两支分别盛有水和澄清石灰水的试管,要求同学们想办法区别,杨新同学立即上台展示了自己的才能,她向两支试管里分别吹气(如图).
化学课上,老师展示了A、B两支分别盛有水和澄清石灰水的试管,要求同学们想办法区别,杨新同学立即上台展示了自己的才能,她向两支试管里分别吹气(如图).(1)A试管出现了浑浊现象,则A试管中的物质是
(2)老师又提出问题:B中是否发生了化学反应?与杨新同组的赵江同学解决了这个问题,他向B中滴入几滴紫色石蕊试液,大家立刻看到溶液变成
考点:碱的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的碱 碱的通性
分析:(1)根据氢氧化钙溶液和二氧化碳反应会生成碳酸钙沉淀和水进行分析;
(2)根据水和二氧化碳反应生成碳酸,碳酸能使紫色石蕊变红色进行分析.
(2)根据水和二氧化碳反应生成碳酸,碳酸能使紫色石蕊变红色进行分析.
解答:解:(1)氢氧化钙溶液和二氧化碳反应会生成碳酸钙沉淀和水,A试管出现了浑浊现象,所以A试管中的物质是澄清石灰水,化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;
(2)通过推导可知,B中的物质是水,水和二氧化碳反应生成碳酸,碳酸能使紫色石蕊变红色,所以向B中滴入几滴紫色石蕊试液,大家立刻看到溶液变成红色,化学方程式为:H2O+CO2=H2CO3.
故答案为:(1)澄清石灰水,Ca(OH)2+CO2=CaCO3↓+H2O;
(2)红,H2O+CO2=H2CO3.
(2)通过推导可知,B中的物质是水,水和二氧化碳反应生成碳酸,碳酸能使紫色石蕊变红色,所以向B中滴入几滴紫色石蕊试液,大家立刻看到溶液变成红色,化学方程式为:H2O+CO2=H2CO3.
故答案为:(1)澄清石灰水,Ca(OH)2+CO2=CaCO3↓+H2O;
(2)红,H2O+CO2=H2CO3.
点评:本题主要考查了二氧化碳的化学性质,以及化学方程式的书写,难度不大,注意平时加强基础知识的记忆.

练习册系列答案
相关题目
 将如图所示装置接通电源,对反应完毕后的有关现象和结论描述正确的是
将如图所示装置接通电源,对反应完毕后的有关现象和结论描述正确的是A.甲试管中收集到的气体能支持燃烧
B.甲、乙两试管中收集到的气体质量比约为2:1
C.甲、乙两试管中收集到的气体体积比约为2:1
D.
RbOH(氢氧化铷)与KOH的性质相似,其碱性比氢氧化钾强,下列有关RbOH性质说法不正确的是( )
| A、氢氧化铷易溶于水 |
| B、氢氧化铷溶液能使紫色石蕊试液变蓝 |
| C、氢氧化铷不能与FeCl3反应 |
| D、氢氧化铷溶液长期露置在空气中会变质 |
 在下列分别盛有不同物质的容器中,所盛物质属于单质的是
在下列分别盛有不同物质的容器中,所盛物质属于单质的是 有A、B、C三种固体物质的溶解度曲线.
有A、B、C三种固体物质的溶解度曲线.