题目内容
 有A、B、C三种固体物质的溶解度曲线.
有A、B、C三种固体物质的溶解度曲线.(1)t1℃时,A、B、C三种物质溶解度由大到小的顺序是
(2)t3℃时,A、B两种物质
(3)t2℃时,B物质饱和溶液的溶质质量分数为
(4)将t1℃时A、B、C三种物质的饱和溶液分别升温到t3℃,有晶体析出的是
考点:固体溶解度曲线及其作用,晶体和结晶的概念与现象,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:(1)据溶解度曲线可比较同一温度下不同物质的溶解度大小;
(2)据饱和溶液中溶质的质量分数计算式
×100%可知:溶解度相等则饱和溶液中溶质的质量分数相等;
(3)据饱和溶液中溶质的质量分数计算方法解答;
(4)C的溶解度随温度升高而减小,升温会析出晶体.
(2)据饱和溶液中溶质的质量分数计算式
| 溶解度 |
| 溶解度+100g |
(3)据饱和溶液中溶质的质量分数计算方法解答;
(4)C的溶解度随温度升高而减小,升温会析出晶体.
解答:解:(1)t1℃时,A、B、C三种物质溶解度由大到小的顺序是B>C>A;
(2)t3℃时AB的溶解度相等,据饱和溶液中溶质的质量分数计算式
×100%可知:溶解度相等则饱和溶液中溶质的质量分数相等,所以A、B两种物质 能形成溶质质量分数相同的饱和溶液;
(3)t2℃时B的溶解度是25g,所以B物质饱和溶液的溶质质量分数为
×100%=20%;
(4)将t1℃时A、B、C三种物质的饱和溶液分别升温到t3℃,C的溶解度随温度升高而减小,有晶体析出;
故答案为:(1)B>C>A;(2)能;(3)20;(4)C.
(2)t3℃时AB的溶解度相等,据饱和溶液中溶质的质量分数计算式
| 溶解度 |
| 溶解度+100g |
(3)t2℃时B的溶解度是25g,所以B物质饱和溶液的溶质质量分数为
| 25g |
| 125g |
(4)将t1℃时A、B、C三种物质的饱和溶液分别升温到t3℃,C的溶解度随温度升高而减小,有晶体析出;
故答案为:(1)B>C>A;(2)能;(3)20;(4)C.
点评:明确溶解度曲线的意义和饱和溶液中溶质的质量分数的计算方法是解答此题的关键因素,考查了学生对知识的掌握和应用.

练习册系列答案
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案
相关题目
分开盛放的A、B两溶液中,共含有Na+、Cu2+、Ba2+、Mg2+、NO3-、OH-、SO42-七种离子.两溶液里所含离子各不相同,已知A溶液里含3种阳离子和2种阴离子,则B溶液里所含离子应该是 .
下列变化中,属于物理变化的是( )
| A、白炽灯泡通电发热 |
| B、食物变质 |
| C、葡萄糖在人体内氧化 |
| D、用富含淀粉的甘薯酿酒 |
只用一种试剂就能将澄清的石灰水、稀硫酸和食盐水三种物质区分开,这种试剂是( )
| A、石蕊试液 |
| B、酚酞试液 |
| C、BaCl2溶液 |
| D、氯化钠溶液 |
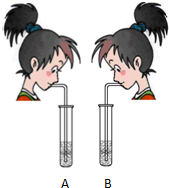 化学课上,老师展示了A、B两支分别盛有水和澄清石灰水的试管,要求同学们想办法区别,杨新同学立即上台展示了自己的才能,她向两支试管里分别吹气(如图).
化学课上,老师展示了A、B两支分别盛有水和澄清石灰水的试管,要求同学们想办法区别,杨新同学立即上台展示了自己的才能,她向两支试管里分别吹气(如图).