题目内容
3.某课外活动小组用化学卡片玩起了趣味的“接龙”游戏.如图是其中一位同学自创的“回龙”谜宫,“--”表示相连的两种物质可以发生反应,“→”表示生成的含义.已知A、B、C、D是NaOH、CuSO4、Fe2O3、HCl四种中的一种,试根据信息回答以下问题:
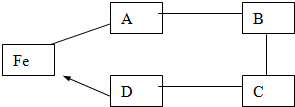
(1)请写出下列物质的化学式:
A.CuSO4 C.HCl
(2)写出下列相关反应的方程式:
D→Fe:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2(合理即可).
分析 根据题意,“--”表示相连的两种物质可以发生反应,“→”表示生成的含义,A、B、C、D是NaOH、CuSO4、Fe2O3、HCl四种中的一种,结合铁能与盐酸、硫酸铜溶液发生置换反应,氧化铁与一氧化碳等还原剂反应生成铁和二氧化碳,则D为氧化铁;氧化铁能与盐酸反应生成氯化铁和水,则C为盐酸,故A为硫酸铜溶液;氢氧化钠能与盐酸发生中和反应生成氯化钠和水,能与硫酸铜溶液反应生成氢氧化铜沉淀和硫酸钠,则B为氢氧化钠溶液;据此进行分析解答.
解答 解:“--”表示相连的两种物质可以发生反应,“→”表示生成的含义,A、B、C、D是NaOH、CuSO4、Fe2O3、HCl四种中的一种,结合铁能与盐酸、硫酸铜溶液发生置换反应,氧化铁与一氧化碳等还原剂反应生成铁和二氧化碳,则D为氧化铁;氧化铁能与盐酸反应生成氯化铁和水,则C为盐酸,故A为硫酸铜溶液;氢氧化钠能与盐酸发生中和反应生成氯化钠和水,能与硫酸铜溶液反应生成氢氧化铜沉淀和硫酸钠,则B为氢氧化钠溶液.
(1)A为硫酸铜溶液,其化学式为:CuSO4;C为盐酸,其化学式为:HCl.
(2)D→Fe,可以通过氧化铁与一氧化碳等还原剂反应生成铁和二氧化碳,反应的化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2(合理即可).
故答案为:(1)CuSO4;HCl;(2)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2(合理即可).
点评 本题难度不大,解题时往往需要从题目中挖出一些明显或隐含的条件,抓住突破口(突破口往往是现象特征、反应特征等),获得结论,最后把结论代入原题中验证.

练习册系列答案
相关题目
14.下列有关硫酸铜及晶体的性质中,属于化学性质的是( )
①.硫酸铜晶体能溶于水 ②.硫酸铜晶体呈蓝色 ③.硫酸铜晶体受热时会从蓝色变为白色 ④.在硫酸铜溶液中滴加氢氧化钠溶液会产生蓝色沉淀.
①.硫酸铜晶体能溶于水 ②.硫酸铜晶体呈蓝色 ③.硫酸铜晶体受热时会从蓝色变为白色 ④.在硫酸铜溶液中滴加氢氧化钠溶液会产生蓝色沉淀.
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
18.区分日常生活中的下列各组物质,操作方法完全正确的是( )
| 需鉴别物质 | 方法Ⅰ | 方法Ⅱ | |
| A | 硫酸铵粉末和碳酸钙粉末 | 加水溶解 | 加熟石灰 |
| B | 一氧化碳和二氧化碳 | 闻气味 | 通过灼热的氧化铜 |
| C | 食盐水和蒸馏水 | 测pH值 | 蒸发结晶 |
| D | 真黄金和假黄金(铜锌合金) | 看颜色 | 灼烧 |
| A. | A | B. | B | C. | C | D. | D |
15. 某化学小组用一定量AgNO3和Al(NO3)3的混合溶液进行了如图实验,已知溶液甲呈蓝色.①向固体乙上滴加盐酸时没有气泡产生;②向固体乙上滴加盐酸时有气泡产生;③溶液甲中一定含有溶质Al(NO3)3、Zn(NO3)2、Cu(NO3)2;④溶液甲中一定不含溶质AgNO3⑤溶液甲中可能含溶质AgNO3.下列说法正确的是( )
某化学小组用一定量AgNO3和Al(NO3)3的混合溶液进行了如图实验,已知溶液甲呈蓝色.①向固体乙上滴加盐酸时没有气泡产生;②向固体乙上滴加盐酸时有气泡产生;③溶液甲中一定含有溶质Al(NO3)3、Zn(NO3)2、Cu(NO3)2;④溶液甲中一定不含溶质AgNO3⑤溶液甲中可能含溶质AgNO3.下列说法正确的是( )
 某化学小组用一定量AgNO3和Al(NO3)3的混合溶液进行了如图实验,已知溶液甲呈蓝色.①向固体乙上滴加盐酸时没有气泡产生;②向固体乙上滴加盐酸时有气泡产生;③溶液甲中一定含有溶质Al(NO3)3、Zn(NO3)2、Cu(NO3)2;④溶液甲中一定不含溶质AgNO3⑤溶液甲中可能含溶质AgNO3.下列说法正确的是( )
某化学小组用一定量AgNO3和Al(NO3)3的混合溶液进行了如图实验,已知溶液甲呈蓝色.①向固体乙上滴加盐酸时没有气泡产生;②向固体乙上滴加盐酸时有气泡产生;③溶液甲中一定含有溶质Al(NO3)3、Zn(NO3)2、Cu(NO3)2;④溶液甲中一定不含溶质AgNO3⑤溶液甲中可能含溶质AgNO3.下列说法正确的是( )| A. | ②③④ | B. | ②④ | C. | ①③④ | D. | ①③⑤ |
12.初中科学课上,同学们利用如图1实验探究碱的化学性质:
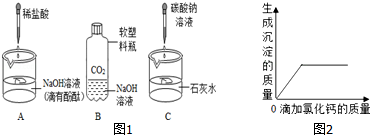
(1)B实验中反应的化学方程式为2NaOH+CO2═Na2CO3+H2O.
(2)C实验中观察到的现象是澄清石灰水变浑浊.
(3)实验结束后,同学们将废液倒入同一只废液缸中,最后发现废液浑浊并显红色.
【提出问题】废液中含有什么物质?
【假设猜想】通过分析上述实验,同学们猜想:废液中除酚酞和水外一定含有NaCl.
老师问:废液中还可能有什么物质?某同学脱口而出:废液中含有氢氧化钠,他的说法正确吗?同学们认为不准确,理由是:Ca(OH)2、Na2CO3溶液也可使酚酞试液变红.于是引发了热烈讨论,下面是大家的发言:
【查阅资料】CaCl2+Na2CO3═CaCO3↓+2NaCl
( 4 )【实验验证】同学们对可能含有的物质进行确定,取一定量的废液过滤,向滤液中逐滴加入氯化钙溶液,根据反应现象绘制了如图2所示的示意图.
①【结论解释】分析图象数据得出可能含有的物质中,一定含有Na2CO3,
②【拓展提高】那么是否含有氢氧化钠呢?请你帮他继续完成实验,写出探究的实验方法:观察沉淀后的溶液的颜色,若溶液变红,则含有NaOH;若溶液不变色,则不含NaOH..

(1)B实验中反应的化学方程式为2NaOH+CO2═Na2CO3+H2O.
(2)C实验中观察到的现象是澄清石灰水变浑浊.
(3)实验结束后,同学们将废液倒入同一只废液缸中,最后发现废液浑浊并显红色.
【提出问题】废液中含有什么物质?
【假设猜想】通过分析上述实验,同学们猜想:废液中除酚酞和水外一定含有NaCl.
老师问:废液中还可能有什么物质?某同学脱口而出:废液中含有氢氧化钠,他的说法正确吗?同学们认为不准确,理由是:Ca(OH)2、Na2CO3溶液也可使酚酞试液变红.于是引发了热烈讨论,下面是大家的发言:
| 学生甲 | 还可能有Ca(OH)2、NaOH | 学生丙 | 还可能有Ca(OH)2、CaCl2 |
| 学生乙 | 还可能有NaOH、Na2CO3 | 学生丁 | 还可能有Na2CO3 |
| … | … |
( 4 )【实验验证】同学们对可能含有的物质进行确定,取一定量的废液过滤,向滤液中逐滴加入氯化钙溶液,根据反应现象绘制了如图2所示的示意图.
①【结论解释】分析图象数据得出可能含有的物质中,一定含有Na2CO3,
②【拓展提高】那么是否含有氢氧化钠呢?请你帮他继续完成实验,写出探究的实验方法:观察沉淀后的溶液的颜色,若溶液变红,则含有NaOH;若溶液不变色,则不含NaOH..
13.下列说法中错误的是( )
| A. | 同种元素组成的物质是单质 | |
| B. | 原子是化学变化中的最小粒子 | |
| C. | 同种分子构成的物质是纯净物 | |
| D. | 元素的化学性质与该元素的原子的最外层电子数关系最密切 |
 A、B、C、D是实验室常见的四种物质,A、B、C在一定条件下的转化关系如图所示.在C溶液中通入CO2,溶液变浑浊,生成白色沉淀A. D与A、B、C均能发生反应,与A反应有CO2气体产生,与C发生中和反应,与AgNO3溶液反应,可产生不溶于稀硝酸的白色沉淀.
A、B、C、D是实验室常见的四种物质,A、B、C在一定条件下的转化关系如图所示.在C溶液中通入CO2,溶液变浑浊,生成白色沉淀A. D与A、B、C均能发生反应,与A反应有CO2气体产生,与C发生中和反应,与AgNO3溶液反应,可产生不溶于稀硝酸的白色沉淀. 在自然界里大多数金属是以化合物的形式存在的.常用的金属冶炼是通过氢气、一氧化碳、碳粉与金属氧化物在高温下反应来实现的.请回答以下有关问题:
在自然界里大多数金属是以化合物的形式存在的.常用的金属冶炼是通过氢气、一氧化碳、碳粉与金属氧化物在高温下反应来实现的.请回答以下有关问题: