题目内容
硫酸亚铁每片中含铁0.56g,每片2.5g.
(1)求硫酸亚铁中铁的质量分数;
(2)求此药片中硫酸亚铁的质量分数;
(3)某患者每天需补充1.4g铁元素,其中80%从这种药剂中补充,问:要服用多少克纯净的硫酸亚铁?
(1)求硫酸亚铁中铁的质量分数;
(2)求此药片中硫酸亚铁的质量分数;
(3)某患者每天需补充1.4g铁元素,其中80%从这种药剂中补充,问:要服用多少克纯净的硫酸亚铁?
考点:元素的质量分数计算,化合物中某元素的质量计算
专题:化学式的计算
分析:(1)根据化合物中元素的质量分数=
×100%,进行分析解答.
(2)根据题意,硫酸亚铁每片中含铁0.56g,每片2.5g,据此结合化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
(3)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
| 相对原子质量×原子个数 |
| 相对分子质量 |
(2)根据题意,硫酸亚铁每片中含铁0.56g,每片2.5g,据此结合化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
(3)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答:解:(1)硫酸亚铁中铁的质量分数为
×100%≈36.8%.
(2)硫酸亚铁每片中含铁0.56g,则每片含硫酸亚铁的质量为0.56g÷(
×100%)=1.52g;每片2.5g,此药片中硫酸亚铁的质量分数为
×100%=60.8%.
(3)某患者每天需补充1.4g铁元素,其中80%从这种药剂中补充,要服用纯净的硫酸亚铁的质量为1.4g×80%÷(
×100%)=0.304g.
答:(1)硫酸亚铁中铁的质量分数为36.8%;(2)此药片中硫酸亚铁的质量分数为60.8%;(3)要服用多少克纯净的硫酸亚铁0.304g.
| 56 |
| 56+32+16×4 |
(2)硫酸亚铁每片中含铁0.56g,则每片含硫酸亚铁的质量为0.56g÷(
| 56 |
| 56+32+16×4 |
| 1.52g |
| 2.5g |
(3)某患者每天需补充1.4g铁元素,其中80%从这种药剂中补充,要服用纯净的硫酸亚铁的质量为1.4g×80%÷(
| 56 |
| 56+32+16×4 |
答:(1)硫酸亚铁中铁的质量分数为36.8%;(2)此药片中硫酸亚铁的质量分数为60.8%;(3)要服用多少克纯净的硫酸亚铁0.304g.
点评:本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下面是学完化学用语后一次学生听写作业的部分内容,其中错误的是( )
| A、3MnO42-:表示3个锰酸根离子 |
B、钠原子结构示意图: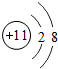 |
| C、Fe3+中的“3”表示每个铁离子带有3个单位的正电荷 |
| D、H2O中的“2”表示一个水分子中含有2个氢原子 |
下列有关催化剂的说法中正确的是( )
| A、MnO2只能作为氧化氢溶液分解的催化剂 |
| B、同一个化学反应可以有多种催化剂 |
| C、催化剂只能加快化学反应的速率 |
| D、用作催化剂的物质不可能是其它反应的反应物或生成物 |