题目内容
我国使用“长征3号甲”运载火箭的动力是由高氯酸铵(NH4ClO4)分解所提供的,反应方程式为2NH4ClO4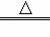
 N2↑+Cl2↑+4X↑+2O2↑,则X的化学式为( )
N2↑+Cl2↑+4X↑+2O2↑,则X的化学式为( )
A.NH3 B.H2 C.H2O D.HCl
【考点】有关化学式的计算和推断;质量守恒定律及其应用.
【分析】根据化学变化前后原子的种类、数目不变,由反应的化学方程式2NH4ClO4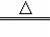
 N2↑+Cl2↑+4X↑+2O2↑,推断反应中生成物X的分子构成,然后确定X物质的化学式.
N2↑+Cl2↑+4X↑+2O2↑,推断反应中生成物X的分子构成,然后确定X物质的化学式.
【解答】解:由反应的化学方程式2NH4ClO4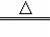
 N2↑+Cl2↑+4X↑+2O2↑,可知:
N2↑+Cl2↑+4X↑+2O2↑,可知:
反应前 反应后
N原子 2 2
H原子 8 0
Cl原子 2 2
O原子 8 4
根据化学变化前后原子的种类、数目不变,可判断生成物X的4个分子中含有8个H原子和4个O原子,则每个X的分子由2个H原子和1个O原子构成,物质X的化学式为H2O;
故选C.

练习册系列答案
相关题目
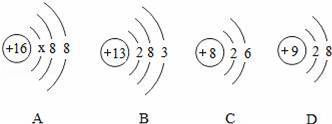

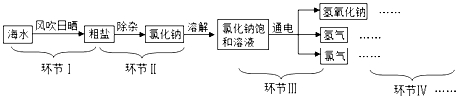
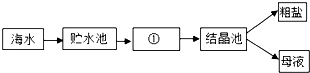
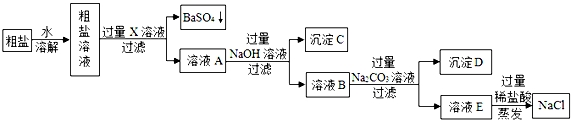

 作业中书写的,请你判断它们是否正确,如有错误,请分别指出错误所在,并书写出正确的方程式。
作业中书写的,请你判断它们是否正确,如有错误,请分别指出错误所在,并书写出正确的方程式。 H2↑+O2↑ ,
H2↑+O2↑ , Hg2+O2↑ ,
Hg2+O2↑ , CO2↑
CO2↑  ,
,