题目内容
9.理性推测是化学研究的一种重要手段.A、B、C是中学化学中常见的化合物,其中C是盐,已知:A+nB=C+H2O (方程式已配平),n为化学计量数.请回答下列问题:(1)当n=1时,B是一种常见的酸,其相对分子质量是98,C的相对分子质量为120.则B的化学式为H2SO4,A的相对分子质量为40,经推测A的化学式为MgO.
(2)当n=2时,请各列举出一个化学反应方程式:若A是一种非金属氧化物SO2、CO2 等;若A是一种金属氧化物CuO或CaO(BaO、MgO)等.
分析 本题也是一道条件开放题.当n=1时,B是一种常见的酸,且其相对分子质量是98,则B的化学式为,根据质量守恒定律可知:A的相对分子质量.该题巧妙的将定量的知识融合到推断中,尤其是将质量守恒定律巧妙的与推断结合是一个较为创新手法.
解答 解:(1)H2SO4是一种常见的酸,且其相对分子质量是98,则B的化学式H2SO4,根据质量守恒定律可知:A的相对分子质量为120+18-98=40;又因为n=1,结合题意可知A为MgO.
(2)当时n=2,若A是一种酸性氧化物,A可为SO2、CO2 等中的一种,它们与可溶性的一元碱(如NaOH、KOH等)反应,反应的化学方程式为2NaOH+CO2=Na2CO3+H2O 或2NaOH+SO2=Na2SO3+H2O或2NaOH+SO3=Na2SO4+H2O;若A是一种碱性氧化物,假设A为CuO或CaO(BaO、MgO)等,可用它们与一元酸(如:HCl、HNO3等)反应,反应的化学方程式可为(以CuO为例):CuO+2HCl=CuCl2+H2O或CaO+2HCl=CaCl2+H2O等.
故答为:(1)H2SO4;40;MgO;
(2)SO2、CO2 等;CuO或CaO(BaO、MgO)等.
点评 推断题主要的核心思想是考查学生整合知识的能力,因此开发网络化的试题,从定性推测向定量推测转化、融合化工生产实际、融合生活实际等是设计的推断题的好途径.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.德国化学家格哈德•埃特尔在固体表面化学的研究中取得了非凡的成就,其成果之一是揭示了氮气与氢气在催化剂表面合成氨的反应过程(如图所示).如图所示微观变化与下列对应叙述正确的是( )


| A. | 此反应有化合物参加 | |
| B. | 原子在化学变化中是可分的 | |
| C. | 符合上述反应过程的顺序是③①② | |
| D. | 对应化学反应方程式为2N+3H2$\frac{\underline{\;催化剂\;}}{\;}$2NH3 |
4.点燃的蜡烛在如图甲所示密闭装置内燃烧一段时间后会自动熄灭,用仪器测出这一过程中瓶内氧气含量的变化如图乙所示.下列判断正确的是( )
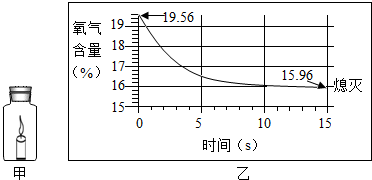

| A. | 蜡烛燃烧前装置内只有氧气 | |
| B. | 蜡烛熄灭后瓶内只剩二氧化碳气体 | |
| C. | 过程中装置内物质总质量不断减少 | |
| D. | 氧气含量小于一定值时,蜡烛无法燃烧 |
4.某金属元素只有一种化合价,它与氯元素形成的化合物的相对分子质量比它与氧元素形成的化合物的相对分子质量大55,则该金属元素的化合价为( )
| A. | +1价 | B. | +2价 | C. | +3价 | D. | 无法确定 |
18.下列微粒符号中,对“2”的含义理解正确的是( )
| A. | 2Cu中的“2”表示2个铜元素 | |
| B. | Fe2+中的“2”表示每个亚铁离子带有2个单位的正电荷 | |
| C. | H2S中的“2”表示1个硫化氢分子中含 有2个硫原子 | |
| D. | S2-表示-2价的硫元素 |
19. 如图是市场充气包装的食品,它使用的是什么气体呢?某兴趣小组对此进行了研究.
如图是市场充气包装的食品,它使用的是什么气体呢?某兴趣小组对此进行了研究.
(1)经访问有关人员,了解到这样包装的目的是为了防止食品挤压变形或食品腐败,且从经济性、环保等因素考虑,工厂使用的包装气体是空气,氮气或二氧化碳.请你以此调查结果为依据,对包装气体的成分提出猜想,并说明你猜想的依据:
(2)请设计实验,检验上述猜想的正确性.填写下列实验报告:
(3)你认为食品充气包装,对所充气体的要求是:①无毒②与食品不反应③价廉易得.
 如图是市场充气包装的食品,它使用的是什么气体呢?某兴趣小组对此进行了研究.
如图是市场充气包装的食品,它使用的是什么气体呢?某兴趣小组对此进行了研究.(1)经访问有关人员,了解到这样包装的目的是为了防止食品挤压变形或食品腐败,且从经济性、环保等因素考虑,工厂使用的包装气体是空气,氮气或二氧化碳.请你以此调查结果为依据,对包装气体的成分提出猜想,并说明你猜想的依据:
| 我对气体的猜想是 | |
| 我猜想的依据是 |
| 实验方法及操作 | 可能观察到的现象及结论 |