题目内容
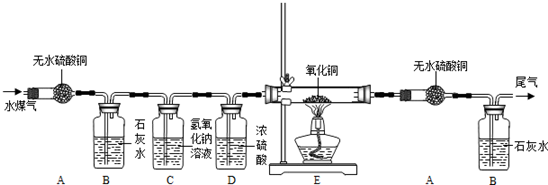
水煤气是将水蒸气通过灼热的焦炭而生成的气体,主要成分是一氧化碳、氢气及少量的二氧化碳和水蒸气。
某课题组同学为验证水煤气的成分,做了以下准备:
[资料收集]①H2+CuO∆Cu+H2O;CO+CuO∆Cu+CO2 ②无 水硫酸铜遇水由白色变为蓝色
水硫酸铜遇水由白色变为蓝色
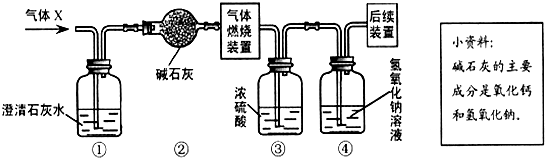
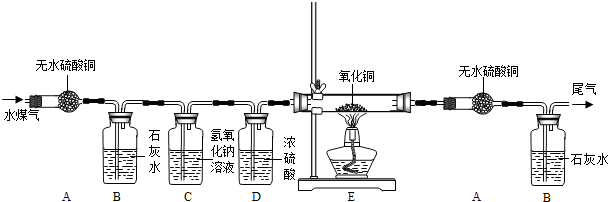
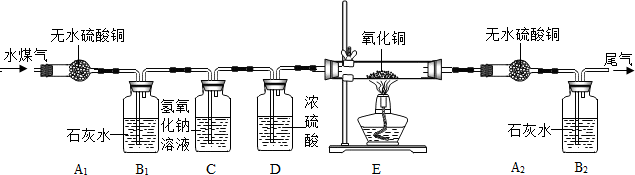
[设计实验装置]
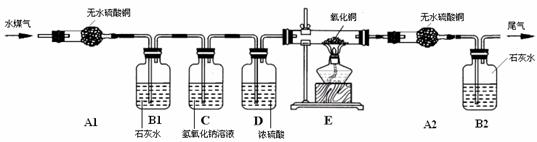 请分析上面信息后回答:
请分析上面信息后回答:
(1)你认为验证水煤气中各成分的顺序依次是 。
(2)装置C的作用是 ,装置D的作用是 。
。
(3)实验中两次用到装置A,其目的分别是A1 , A2: 。
(4)请你设计一种尾气处理方案: 。
(5)可以通过测量反应前后E处大玻璃管的质量变化,来计算氧化铜的纯度(杂质只有铜)。在这个实验装置中,除了这种方法外,你认为还可以通过测量来计算氧化铜样品纯度的方法是 。
(1)水蒸气、二氧化碳、氢气、一氧化碳(用化学式表示亦可,顺序错 不得分)(2)除去水煤气中的二氧化碳;除去水煤气中和装置B、C中引入的水蒸气(或除去水蒸气或干
不得分)(2)除去水煤气中的二氧化碳;除去水煤气中和装置B、C中引入的水蒸气(或除去水蒸气或干 燥混合气体)(3)验证水煤气中水蒸气的存在;检验水煤
燥混合气体)(3)验证水煤气中水蒸气的存在;检验水煤 气中是否含有氢气(4)在装置最后用燃着的酒精灯引燃或用气球收集(5)测量反应前后A2、B2的质量变化来计算氧化铜样品的纯度(A2、B2缺一不得分)
气中是否含有氢气(4)在装置最后用燃着的酒精灯引燃或用气球收集(5)测量反应前后A2、B2的质量变化来计算氧化铜样品的纯度(A2、B2缺一不得分)

练习册系列答案
相关题目