题目内容
18.为了减少城市酸雨的产生,可采取的措施是( )| A. | 少用煤作燃料 | B. | 采用燃料脱硫技术 | ||
| C. | 向已酸化的土壤中加熟石灰 | D. | 开发新源 |
分析 少用煤作燃料、燃料脱硫、开发新的能源等措施可以减少二氧化硫气体的排放,从而减少酸雨的形成;把工厂烟囱造高,不能减少二氧化硫的生成,则无法有效地防止酸雨的形成.
解答 解:A、少用煤作燃料,可以减少二氧化硫气体的排放,从而减少了酸雨的形成,可行;
B、燃料脱硫,可以减少二氧化硫气体的排放,从而减少了酸雨的形成,可行;
C、向已酸化的土壤中加熟石灰,不能减少酸雨,不可行;
D、开发新的能源,可以减少二氧化硫气体的排放,从而减少了酸雨的形成,可行.
故选ABD.
点评 本题主要考查酸雨形成的原因及防治措施,题目难度不大,明确酸雨的形成原因为解答关键,注意了解酸雨的危害及治理方法,试题侧重基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
相关题目
8.下列有关物质的分类错误的是( )
| A. | 生石灰属于氧化物 | B. | 小苏打属于盐 | ||
| C. | 干冰属于混合物 | D. | 氩气属于单质 |
6.关于物质性质及用途的描述中错误的是( )
| A. | 熟石灰呈碱性,可用于改良酸性土壤 | |
| B. | 干冰气化吸热,可用于人工降雨 | |
| C. | 氧气有助燃性,可用于炼铜和气焊 | |
| D. | 稀有气体性质稳定,可制成霓虹灯 |
13.实验室有碳酸钡和碳酸钙的固体混合物50g,与足量盐酸充分反应,将反应后的溶液蒸干得到53.3g固体,则原混合物中金属元素的质量分数为( )
| A. | 64% | B. | 40% | C. | 36% | D. | 69.5% |
3.下列粒子结构示意图中,表示阴离子的是( )
| A. | 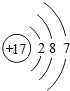 | B. |  | C. |  | D. |  |