题目内容
17.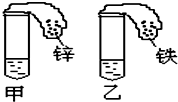 如图所示,在试管和小气球中分别先加入浓度、质量均相等的足量稀硫酸和等质量的金属锌、铁,然后将气球中的金属倒入试管中,观察到的现象是:试管中有气泡产生,开始时,甲气球迅速鼓起,而乙气球鼓起较慢;反应结束后,甲气球体积比乙气球小(填:大、小、一样大)
如图所示,在试管和小气球中分别先加入浓度、质量均相等的足量稀硫酸和等质量的金属锌、铁,然后将气球中的金属倒入试管中,观察到的现象是:试管中有气泡产生,开始时,甲气球迅速鼓起,而乙气球鼓起较慢;反应结束后,甲气球体积比乙气球小(填:大、小、一样大)
分析 根据金属活动性顺序可知,锌比铁活泼,与酸反应生成氢气的速率快,锌的相对原子质量大于铁,所以等质量的金属锌、铁与浓度、质量均相等的足量稀硫酸反应,铁生成的氢气多进行分析.
解答 解:根据金属活动性顺序可知,锌比铁活泼,与酸反应生成氢气的速率快,锌的相对原子质量大于铁,所以等质量的金属锌、铁与浓度、质量均相等的足量稀硫酸反应,铁生成的氢气多,所以开始时,甲气球迅速鼓起,而乙气球鼓起较慢;反应结束后,甲气球体积比乙气球小.
故答案为:甲,乙,小.
点评 本题主要考查了金属活动性顺序的应用,难度不大,需要在平时多加记忆.

练习册系列答案
相关题目
12.某课外活动小组的同学对一批钢铁样品(含杂质,杂质不溶于水,也不与稀硫酸反应)进行分析,甲、乙、丙三位同学分别进行了实验,其中只有一位同学所取的稀硫酸与样品恰好完全反应,实验数据如下:
请你根据所给数据,回答下列问题:
(1)所取的稀硫酸与钢铁样品恰好完全反应的是乙同学.
(2)该钢铁样品中含铁的质量分数为多少?
| 甲 | 乙 | 丙 | |
| 烧杯+稀硫酸 | 200g | 150g | 150g |
| 加入的钢铁样品 | 9g | 9g | 14g |
| 充分反应后,烧杯+剩余物 | 208.7g | 158.7g | 163.7g |
(1)所取的稀硫酸与钢铁样品恰好完全反应的是乙同学.
(2)该钢铁样品中含铁的质量分数为多少?
2.下列事实不能证明金属甲的金属活动性比金属乙强的是( )
| A. | 自然界中甲元素只以化合物形式存在,乙元素存在单质形式 | |
| B. | 甲能与盐酸反应生成H2而乙不能 | |
| C. | 甲能从乙的盐溶液中置换出乙 | |
| D. | 化合物中甲元素显+2价而乙元素显+3价 |
6.下列有关水和溶液的说法中正确的是( )
| A. | 凡是均一、稳定的液体都是溶液 | |
| B. | 电解水时产生的氢气和氧气的质量比为2:1 | |
| C. | 相同温度下,饱和溶液一定比不饱和溶液浓 | |
| D. | 可用肥皂水可以区分软水和硬水 |
 根据图中甲.乙两种物质的溶解度曲线,回答下列问题.
根据图中甲.乙两种物质的溶解度曲线,回答下列问题.