题目内容
12.车用乙醇汽油是将乙醇(C2H5OH)与汽油按一定比例混合而成的一种汽车燃料.①在密闭容器中,将少量乙醇置于一定量氧气中燃烧,生成二氧化碳、水蒸气和一种未知物质w.现测得反应前后各物质的质量如下:
| 物质 | 乙 醇 | 氧 气 | 二氧化碳 | 水蒸气 | w |
| 反应前质量/g | 23 | 40 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 22 | 27 | x |
②根据表中数据,可确定未知物w中所含C、O元素,其组成元素的质量比为3:4;
③为了使乙醇汽油燃烧过程中少产生w,应采取的措施是加大空气的进入量(任写一种).
分析 ①欲正确解答本题,须根据质量守恒定律,反应前物质的质量=反应后物质的质量进行计算;
②欲正确解答本题,需根据化学方程式配平的原则,写出方程式,即可得出W的化学式,然后根据化学式进行计算即可.
③欲正确解答本题,须知CO气体的产生与什么有关,进而采取相应的措施.
解答 解:①根据质量守恒定律,反应前物质的质量=反应后物质的质量.故x=23g+40g-(22g+27g)=14g,故答案为:14.
②根据乙醇和氧气的质量关系和化学方程式配平的原则可得反应的化学方程式为:2C2H5OH+5O2$\frac{\underline{\;点燃\;}}{\;}$6H2O+2CO2+2CO,故未知物w中所含的元素为C、O;其组成元素的质量比为12:16=3:4.故填:C、O,3:4.
③在反应过程中之所以生成CO气体,是因为燃烧不充分,要使乙醇汽油燃烧过程中少产生CO气体,需加大空气的进入量,在氧气充足的情况下让其充分燃烧.故答案为:加大空气的进入量.
点评 本题考查学生对有机物和无机物的概念和区别、质量守恒定律、化学方程式配平的原则的认识,以及运用化学式进行计算的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.久装石灰水的试剂瓶瓶壁上有一层白膜(主要成分是碳酸钙),为去掉白膜,加稀盐酸,有气泡,该气泡是( )
| A. | 氧气 | B. | 二氧化碳 | C. | 氢气 | D. | 氮气 |
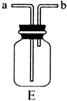 如图所示为实验室中常见的气体制备和收集装置.请回答:
如图所示为实验室中常见的气体制备和收集装置.请回答: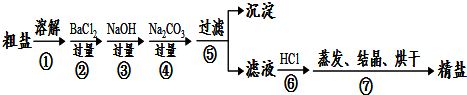
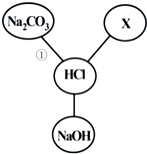 盐酸既是盐化工的重要产品,又是生产硅材料的重要原料.如图归纳出了盐酸与其他物质间相互反应的关系(图中“-”表示相连的两种物质能发生反应).
盐酸既是盐化工的重要产品,又是生产硅材料的重要原料.如图归纳出了盐酸与其他物质间相互反应的关系(图中“-”表示相连的两种物质能发生反应). 根据化学式计算:
根据化学式计算: 如图为电解水的装置,根据观察到的实验现象回答:
如图为电解水的装置,根据观察到的实验现象回答: