题目内容
2.请结合如图1回答问题: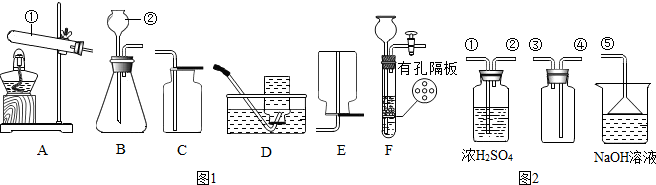
(1)写出有标号的仪器名称:②长颈漏斗.
(2)实验室用高锰酸钾制取O2的化学方程式为2KMn04$\frac{\underline{\;\;△\;\;}}{\;}$K2Mn04+Mn02+02↑.
(3)实验室制取CO2若将发生装置由B改为F,其优点是可以控制反应的开始和停止.
(4)SO2是无色有刺激性气味的有毒气体,密度比空气大,易溶于水,SO2的某些化学性质与CO2相似,实验中常用NaOH溶液吸收SO2尾气生成亚硫酸钠(Na2SO3)和水.用如图2所示装置收集一瓶干燥的SO2,装置中导管按气流方向连接顺序是①→②→④③⑤(填序号);烧杯中NaOH溶液的作用是2NaOH+SO2=Na2SO3+H2O(用化学方程式表示).
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气进行分析;
(3)根据该装置可以利用生成气体的用压强将固体和液体隔离,来达到是反应停止进行分析;
(4)根据二氧化硫的密度比空气大,有毒,二氧化硫和氢氧化钠反应生成亚硫酸钠和水进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,②是长颈漏斗;
(2)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMn04$\frac{\underline{\;\;△\;\;}}{\;}$K2Mn04+Mn02+02↑;
(3)该装置可以利用生成气体的用压强将固体和液体隔离,来达到是反应停止,所以优点是可以控制反应的开始和停止;
(4)二氧化硫的密度比空气大,有毒,所以装置中导管按气流方向连接顺序是①→②→④③⑤;烧杯中NaOH溶液的作用是吸收二氧化硫,二氧化硫和氢氧化钠反应生成亚硫酸钠和水,化学方程式为:2NaOH+SO2=Na2SO3+H2O.
故答案为:(1)长颈漏斗;
(2)2KMn04$\frac{\underline{\;\;△\;\;}}{\;}$K2Mn04+Mn02+02↑;
(3)可以控制反应的开始和停止;
(4)④③;2NaOH+SO2=Na2SO3+H2O.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

练习册系列答案
 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案
相关题目
12.FeS,FeSO3,FeSO4组成的混合物中,氧元素的质量分数为x,则铁的质量分数为( )
| A. | (1-x)×$\frac{4}{11}$ | B. | (1-x)×$\frac{1}{7}$ | C. | (1-x)×$\frac{7}{11}$ | D. | (1-x)×$\frac{1}{11}$ |
10.铬(Cr)为不锈钢主要的添加的元素,含量一般在12%以上.铬的表面上生成一薄层致密的钝态氧化物保护膜是不锈钢具有耐蚀性主要原因.请回答下列问题:
(1)铁生锈的主要条件是铁与O2和H2O直接接触.
(2)不锈钢属于金属材料( 填“合成材料”或“金属材料”).
(3)相同温度下,取大不相同、表面光亮的Cr、Mg、Cu三种金属薄片,分别投入等体积等溶质质量分数的足量稀盐酸中(生成物中Cr显+2价),现象如下:
①上述三种金属的活动性由强到弱的顺序是Mg>Cr>Cu.
②从上述实验可知,Cr能跟CuSO4溶液反应,请写出反应的化学程式Cr+CuSO4=CrSO4+Cu.
(1)铁生锈的主要条件是铁与O2和H2O直接接触.
(2)不锈钢属于金属材料( 填“合成材料”或“金属材料”).
(3)相同温度下,取大不相同、表面光亮的Cr、Mg、Cu三种金属薄片,分别投入等体积等溶质质量分数的足量稀盐酸中(生成物中Cr显+2价),现象如下:
| 金属 | Cr | Mg | Cu |
| 与盐酸反应现象 | 放出气泡速率缓慢 | 放出气泡速率较快 | 无明显现象 |
②从上述实验可知,Cr能跟CuSO4溶液反应,请写出反应的化学程式Cr+CuSO4=CrSO4+Cu.
17.在灾区为防止疾病传染,需对河水处理后方可引用,常用的措施有( )
①加热煮沸 ②消毒 ③过滤④自然沉降,较合理的顺序为.
①加热煮沸 ②消毒 ③过滤④自然沉降,较合理的顺序为.
| A. | ③①②④ | B. | ④①③② | C. | ④③②① | D. | ③①④② |
7.下列有关金属的说法错误的是( )
| A. | 金属的回收利用是保护金属资源的有效途径之一 | |
| B. | 炒完菜后应及时除掉锅底的水,这样可以防止铁锅生锈 | |
| C. | 铝在空气中易生成一层致密的氧化物保护膜,故铝制品性质不稳定 | |
| D. | 生铁和钢是含碳量不同的铁合金,其中生铁的含碳量大于钢的含碳量 |
14.为测定某化肥[(NH4)2SO4和NH4Cl组成]的含氮量,取11g于研钵中,向其中加入氢氧化钙充分反应,当加入7.4g氢氧化钙时恰好完全反应,则此化肥中氮元素的质量分数约为( )
| A. | 14% | B. | 28% | C. | 23.3% | D. | 25.5% |
11.下列属于复合肥料的是( )
| A. | NaNO3 | B. | K2SO4 | C. | NH4H2PO4 | D. | Ca3(PO4)2 |
12.下列各项实验(括号内为相应的操作或方法),能达到实验目的是( )
| A. | 除去CO2中的少量CO(点燃) | |
| B. | 验证硫酸铵溶液(取样,加氢氧化钠溶液) | |
| C. | 检验CaO中混有的CaCO3溶液(滴加稀盐酸) | |
| D. | 鉴别氢氧化钠和碳酸钠(取样,溶解,滴加酚酞) |