题目内容
10.铬(Cr)为不锈钢主要的添加的元素,含量一般在12%以上.铬的表面上生成一薄层致密的钝态氧化物保护膜是不锈钢具有耐蚀性主要原因.请回答下列问题:(1)铁生锈的主要条件是铁与O2和H2O直接接触.
(2)不锈钢属于金属材料( 填“合成材料”或“金属材料”).
(3)相同温度下,取大不相同、表面光亮的Cr、Mg、Cu三种金属薄片,分别投入等体积等溶质质量分数的足量稀盐酸中(生成物中Cr显+2价),现象如下:
| 金属 | Cr | Mg | Cu |
| 与盐酸反应现象 | 放出气泡速率缓慢 | 放出气泡速率较快 | 无明显现象 |
②从上述实验可知,Cr能跟CuSO4溶液反应,请写出反应的化学程式Cr+CuSO4=CrSO4+Cu.
分析 (1)根据已有的铁生锈的条件分析解答,铁在与水和氧气并存时易生锈,防锈就是破坏铁生锈的条件,据此解答.
(2)金属材料包括纯金属和合金;
(3)①根据金属和酸反应的现象进行分析;
②根据判断出的金属活动性顺序进行分析书写.
解答 解:(1)铁在与水和氧气并存时易生锈,故填:O2、H2O;
(2)不锈钢是铁的合金,属于金属材料故填:金属材料;
(3)①镁和盐酸反应放出气泡较快,说明镁最活泼,铜和盐酸反应无现象,说明铜最不活泼,铬与盐酸反应放出气泡较慢,说明介于镁和铜之间,故答案为:Mg>Cr>Cu;
②通过判断可知铬比铜活泼,可以将铜从其盐溶液中置换出来,故答案为:Cr+CuSO4=CrSO4+Cu.
点评 在解此类题时,首先分析题中的问题,然后结合题中所给的知识和学过的知识进行分析解答.

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目
1.验证铁的金属活动性比铜强,下列各组药品能达到目的是( )
| A. | Fe、Cu、ZnSO4 | B. | Fe、Cu、H2SO4 | C. | Ag、CuSO4、FeSO4 | D. | Fe、Cu、KOH |
18.分类法是一种行之有效、简单易行的科学方法.某同学用下表所示形式对所学知识进行分类,其中甲与乙、丙、丁是包含关系.下列各组中,分类有错误的是( )
| 选项 | 甲 | 乙、丙、丁 |
| A | 常见可燃性气体 | 氢气、甲烷、一氧化碳 |
| B | 常见碱 | 烧碱、纯碱、熟石灰 |
| C | 常见营养物质 | 蛋白质、维生素、无机盐 |
| D | 常见合成材料 | 塑料、合成纤维、合成橡胶 |
| A. | A | B. | B | C. | C | D. | D |
5.环境问题已成为制约社会发展和进步的严重问题,下列说法不正确的是( )
| A. | 大量使用农药、化肥以提高农作物产量 | |
| B. | 氟利昂的大量使用将造成臭氧空洞 | |
| C. | 大量使用塑料制品会造成白色污染 | |
| D. | 随意排放工厂废水造成水体污染 |
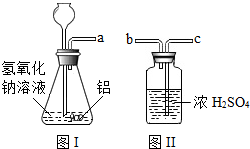 实验中,小红误将氢氧化钠溶液当酸滴加到金属铝中,结果发现也有气泡产生,为了解该气体的成分,实验小组进行了以下探究活动:
实验中,小红误将氢氧化钠溶液当酸滴加到金属铝中,结果发现也有气泡产生,为了解该气体的成分,实验小组进行了以下探究活动: