题目内容
18.如图为四种粒子的结构示意图,请用对应的序号填空.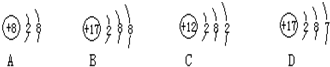
(1)属于同种元素的粒子是BD;
(2)具有相对稳定结构的粒子是AB;
(3)属于原子的粒子是C;
(4)属于阴离子的是B;
(5)容易失电子的是C.
分析 根据已有的知识进行分析,核内质子数相同的微粒则属于同种元素,最外层电子数为8的结构具有稳定结构(氦为2个),在阳离子中,核内质子数大于核外电子数,最外层电子数小于4的易失去电子据此解答.
解答 解:(1)B和D的核内质子数相同,属于同种元素,故填:BD;
(2)A和B的最外层电子数是8,具有稳定的机构,故填:AB;
(3)在C中质子数等于电子数,属于原子,故填C;
(4)B中的核内质子数小于核外电子数,表示的是阴离子,故填:B.
(5)在C中,最外层电子数是3,小于4,在化学反应中容易失电子,故填:C.
点评 本题考查了的是原子结构的有关知识,完成此题,可以依据已有的知识结合图示进行.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
8.鉴别三瓶无色气体氧气、空气和二氧化碳,需要( )
| A. | 带火星的木条 | B. | 澄清的石灰水 | C. | 闻气味 | D. | 燃烧的木条 |
6.某校“酸雨”(pH<5.6)测量小组的同学,取刚降落的雨水的水样,用pH计每隔五分钟测一次pH,其数据见下表:
(1)根据所学知识,推测出“正常雨水”的pH<7,引起这种pH的原因是:二氧化碳溶于雨水形成碳酸;
(2)根据以上数据,判断所降雨水是否为“酸雨”?是
(3)酸雨对农作物以及一些建筑物等不利,请你写出一点减少酸雨的合理意见:使用脱硫煤、硫酸厂排出的废气处理后再排放.
| 测定时间 | 3:10 | 3:15 | 3:20 | 3:25 | 3:30 | 3:35 | 3:40 |
| pH | 4.95 | 4.95 | 4.94 | 4.88 | 4.86 | 4.85 | 4.84 |
(2)根据以上数据,判断所降雨水是否为“酸雨”?是
(3)酸雨对农作物以及一些建筑物等不利,请你写出一点减少酸雨的合理意见:使用脱硫煤、硫酸厂排出的废气处理后再排放.
3.下列对应关系不正确的是( )
| A. | 道尔顿--原子论 | B. | 阿伏加德罗--分子学说 | ||
| C. | 门捷列夫--元素周期表 | D. | 道尔顿--绿色化学 |
7.实验室常用如图所示装置来制取氧气:

(1)用氯酸钾制取氧气时,发生反应的文字表达式为氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气.
(2)用E装置收集氧气时,检验氧气是否集满的方法是将带火星的木条放在集气瓶口,若木条复燃,则证明已收集满.
(3)用双氧水和二氧化锰来制取氧气时,可选用的发生装置是B(填序号),其中二氧化锰起催化作用,该反应的文字表达式为过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.
对此实验,让我们继续思考并研究几个问题:
问题①:催化剂二氧化锰(MnO2)的用量对反应速率有没有影响?
我的实验方案是:每次均用30mL10%的过氧化氢(H2O2)溶液,采用不同量二氧化锰(MnO2)粉末作催化剂,测定各次收集到500mL氧气时所用的时间,结果如下:(其他条件均相同)
请你分析表中数据并回答:MnO2的用量对反应速率有无影响,如果有,怎样影响?催化剂越多,生成相同体积的气体所需时间越短,反应越快.

(1)用氯酸钾制取氧气时,发生反应的文字表达式为氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气.
(2)用E装置收集氧气时,检验氧气是否集满的方法是将带火星的木条放在集气瓶口,若木条复燃,则证明已收集满.
(3)用双氧水和二氧化锰来制取氧气时,可选用的发生装置是B(填序号),其中二氧化锰起催化作用,该反应的文字表达式为过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.
对此实验,让我们继续思考并研究几个问题:
问题①:催化剂二氧化锰(MnO2)的用量对反应速率有没有影响?
我的实验方案是:每次均用30mL10%的过氧化氢(H2O2)溶液,采用不同量二氧化锰(MnO2)粉末作催化剂,测定各次收集到500mL氧气时所用的时间,结果如下:(其他条件均相同)
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 二氧化锰(MnO2)粉末用量(g) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 |
| 所用时间(t) | 17 | 8 | 7 | 5 | 4 | 3 | 2 | 2 |

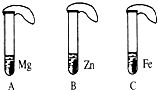 一般情况下,金属越活泼,与酸反应速度越快.为了探究金属Mg、Zn、Fe与酸反
一般情况下,金属越活泼,与酸反应速度越快.为了探究金属Mg、Zn、Fe与酸反