题目内容
15.氯化钠是食盐的主要成分,在自然界中分布很广,食盐还是生产、生活中常见的物质,常用于生产氯气、烧碱、做调味品等.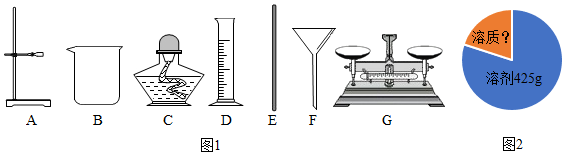
请回答下列问题:
(1)海水晒盐可以获得食盐的道理是蒸发结晶.
(2)除去海盐中含有的泥沙方法如下:
①称量与溶解,需用仪器标号是GDBE.
②过滤,观察过滤后所得溶液仍有些浑浊,写出一点在实验过程中错误的操作液面高于滤纸边缘.
③蒸发.将再过滤后得到的无色透明滤液小心转移到蒸发皿中进行蒸发,当蒸发皿中出现较多固体时,停止加热,利用余热将滤液蒸干.
④用玻璃棒将固体转移,比较食盐提纯前后的状态,得到的精盐是混合物(填“纯净物”或“混合物”).
(3)威威需用15%的氯化钠溶液帮爷爷挑选种子,根据如图2编制一道计算题并解答.
(4)以化学的名义从不同思维角度简要说明区别蒸馏水和氯化钠溶液的实验方案.
⑤分别蒸发液体,能够留下固体的是氯化钠溶液,完全消失的是蒸馏水;
⑥分别尝味道,有咸味的是氯化钠溶液,没有味道的是蒸馏水;
⑦分别加入适量硝酸银溶液,产生白色沉淀的是氯化钠溶液,无明显现象的是蒸馏水.
分析 (1)海水晒盐可以获得食盐的道理是:通过蒸发水使氯化钠的质量分数不断增大,达到饱和溶液时,继续蒸发水时会析出氯化钠;
(2)利用托盘天平可以称量氯化钠质量,利用量筒可以量取水,利用水、烧杯和玻璃棒可以溶解氯化钠;
滤纸破裂、液面高于滤纸边缘时,会导致滤液浑浊;
蒸发时,当蒸发皿中出现较多固体时,停止加热,利用余热将滤液蒸干;
比较食盐提纯前后的状态,得到的精盐中仍然含有一些溶于水的物质,属于混合物;
(3)根据提供的信息可以编制计算题;
(4)利用物理方法和化学方法都能够区分蒸馏水和氯化钠溶液.
解答 解:(1)海水晒盐可以获得食盐的道理是蒸发结晶.
故填:蒸发结晶.
(2)①称量与溶解时,利用托盘天平可以称量氯化钠质量,利用量筒可以量取水,利用水、烧杯和玻璃棒可以溶解氯化钠,因此需用仪器标号是GDBE.
故填:GDBE.
②过滤后,观察过滤后所得溶液仍有些浑浊,实验过程中错误的操作可能是液面高于滤纸边缘.
故填:液面高于滤纸边缘.
③蒸发时,当蒸发皿中出现较多固体时,停止加热,利用余热将滤液蒸干.
故填:出现较多固体时.
④比较食盐提纯前后的状态,得到的精盐是混合物,这是因为其中含有一些溶于水的杂质.
故填:混合物.
(3)已知溶剂质量是425g,溶质质量分数是15%,求该溶液中的溶质质量.
解:设溶质质量为x,
根据题意有:$\frac{x}{x+425g}$×100%=15%,
x=75g,
答:溶液中的溶质质量是75g.
(4)实验方案:
方案一:分别蒸发液体,能够留下固体的是氯化钠溶液,完全消失的是蒸馏水;
方案二:分别尝味道,有咸味的是氯化钠溶液,没有味道的是蒸馏水;
方案三:分别加入适量硝酸银溶液,产生白色沉淀的是氯化钠溶液,无明显现象的是蒸馏水.
故填:分别蒸发液体,能够留下固体的是氯化钠溶液,完全消失的是蒸馏水;分别尝味道,有咸味的是氯化钠溶液,没有味道的是蒸馏水;分别加入适量硝酸银溶液,产生白色沉淀的是氯化钠溶液,无明显现象的是蒸馏水.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

 名校课堂系列答案
名校课堂系列答案| A. | 氯化钠 | B. | 硝酸铵 | C. | 氢氧化钠 | D. | 蔗糖 |
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向食醋中加入氢氧化钠溶液 | 无明显现象 | 二者之间不发生反应 |
| B | 向红墨水中加入活性炭,过滤 | 红墨水变无色 | 活性炭具有吸附性 |
| C | 用黄铜片在铜片上刻划 | 铜片上有划痕 | 黄铜的硬度比铜大 |
| D | 电解水 | 电极上有气泡产生 | 水电解有气体生成 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 氧化铜、木炭粉 | B. | 碳酸钙、氯化钙 | C. | 硝酸钾、氯化钠 | D. | 酒精、水 |

 用相同质量的铁和锌跟一定量的稀硫酸反应,其反应过程如图所示.试回答:
用相同质量的铁和锌跟一定量的稀硫酸反应,其反应过程如图所示.试回答: