题目内容
已知t℃时,KNO3的溶解度为25g.先将15g KNO3与50g水充分混合,得到该温度下的KNO3溶液Mg,该溶液的KNO3质量分数为N%,则可断定( )
| A、M=65,N=20 |
| B、M=65,N=25 |
| C、M=62.5,N=20 |
| D、M<62.5,N<20 |
考点:固体溶解度的概念,有关溶质质量分数的简单计算
专题:溶液、浊液与溶解度
分析:溶解度是指:在一定温度下,某固体物质在100克溶剂里达到饱和状态所溶解的质量.已知t℃时,KNO3的溶解度为25g,因此50g水中溶解12.5g硝酸钾恰好达到饱和状态,因此得到该温度下的KNO3溶液M=12.5g+50g=62.5g;该溶液的KNO3质量分数=
×100%=20%.
| 12.5g |
| 62.5g |
解答:解:A、M=12.5g+50g=62.5g,N=20%,故选项错误;
B、M=12.5g+50g=62.5g,N=20%,故选项错误;
C、已知t℃时,KNO3的溶解度为25g,因此50g水中溶解12.5g硝酸钾恰好达到饱和状态,因此得到该温度下的KNO3溶液M=12.5g+50g=62.5g;该溶液的KNO3质量分数=
×100%=20%,故选项正确;
D、M=12.5g+50g=62.5g,N=20%,故选项错误;
故选C
B、M=12.5g+50g=62.5g,N=20%,故选项错误;
C、已知t℃时,KNO3的溶解度为25g,因此50g水中溶解12.5g硝酸钾恰好达到饱和状态,因此得到该温度下的KNO3溶液M=12.5g+50g=62.5g;该溶液的KNO3质量分数=
| 12.5g |
| 62.5g |
D、M=12.5g+50g=62.5g,N=20%,故选项错误;
故选C
点评:本考点考查了固体物质的溶解度,溶解度的概念有四个要点:①指明温度;②100克溶剂;③达到饱和状态;④质量即单位是克.有关的计算要准确,本考点是中考的一个重要考点,一定要加强记忆,理解应用.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案
相关题目
密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:
下列说法正确的是( )
| 物 质 | A | B | C | D |
| 反应前质量(g) | 5.3 | 8.4 | 1.0 | 2.4 |
| 反应后质量(g) | 10.6 | 0 | 1.9 | 待测 |
| A、该反应为化合反应 |
| B、反应后生成D的质量为4.6g |
| C、反应过程中,物质C与物质D变化的质量比为9:22 |
| D、若物质A与物质B相对分子质量之比为53:42,反应中A与B的化学计量数之比为1:1 |
陈超在实验室发现一瓶标签残缺的无色溶液如图,这瓶溶液可能是( )


| A、氯化钾 | B、氢氧化钾 |
| C、硫酸钾 | D、硝酸钾 |
水是生命之源节约保护水资源是每个公民应尽的义务.下列说法或做法正确的是( )
| A、利用过滤的方法可将硬水转化为软水 |
| B、保护水资源,禁止使用化肥、农药 |
| C、为节约用水,用工业废水直接灌溉农田 |
| D、城市浇水,使用喷灌、滴灌技术 |
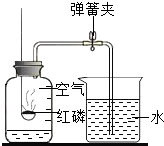 如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号.下列说法中不正确的是( )
如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号.下列说法中不正确的是( )A、该实验证明空气中氧气的含量约占
| ||
| B、实验时红磷一定要足量 | ||
| C、实验前一定要检验装置的气密性 | ||
| D、红磷燃烧产生大量的白雾,火焰熄灭后并冷却后打开弹簧夹 |
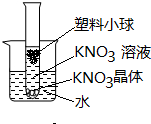 如图所示,烧杯中盛有一定量的水,试管中盛有一定量的有少量固体存在的硝酸钾溶液,在溶液中悬浮着一只塑料小球,请回答下面问题.
如图所示,烧杯中盛有一定量的水,试管中盛有一定量的有少量固体存在的硝酸钾溶液,在溶液中悬浮着一只塑料小球,请回答下面问题.