题目内容
17.性质决定用途,下列物质的用途主要由物理性质决定的是( )| A. | 干冰用于人工降雨 | B. | 镁粉用于制作照明弹 | ||
| C. | 小苏打用于治疗胃酸过多 | D. | 熟石灰用于改良酸性土壤 |
分析 物质的化学性质是指在化学变化中表现出来的性质,物质的物理性质是指不需要通过化学变化表现出来的性质,据此进行分析判断.
解答 解:A、干冰用于人工降雨是利用干冰升华吸热,空气中水蒸气冷凝成水滴,利用的是物理性质,故A正确;
B、镁粉用于制作照明弹,是利用了镁燃烧能发出耀眼强光的性质,需要通过化学变化才表现出来,是利用了其化学性质,故B错;
C、小苏打用于治疗胃酸过多,需要通过化学变化才表现出来,是利用了其化学性质,故C错;
D、氢氧化钙具有碱性,能和酸性物质反应,可用于改良酸性土壤,利用了其化学性质,故D错.
故选A.
点评 物理性质、化学性质是一对与物理变化、化学变化有密切关系的概念,联系物理变化、化学变化来理解物理性质和化学性质,则掌握起来并不困难.

练习册系列答案
相关题目
7.为了防止实验室意外事故的发生,下列预处理方法中错误的是( )
| 选项 | 需预防的意外 | 预处理方法 |
| A | 打翻燃着的酒精灯 | 备湿抹布用来灭火 |
| B | 使用玻璃管时划伤手指 | 将玻璃管口熔圆并备好创可贴 |
| C | 铁丝在氧气中燃烧时炸裂瓶底 | 预先在集气瓶里放少量水或细沙 |
| D | 做CO还原CuO实验时有CO泄露 | 教室内多摆水盆吸收空气中的CO |
| A. | A | B. | B | C. | C | D. | D |
8.有一种标签破损的片状胃药,某校化学兴趣小组欲对该胃药的主要成分进行实验探究.已知该胃药可以治疗胃酸过多,其主要成分是MgCO3、Al(OH)3中的一种或二种.
【查阅资料】①MgCO3受热能分解,且MgCO3的化学性质与CaCO3相似;
②Al(OH)3受热分解生成Al2O3和H2O;③药品中的其它成分不参与反应.
【实验探究】
(1)甲同学取少量该胃药于试管中,加入适量稀盐酸,观察到有气泡产生.说明该胃药中含有MgCO3或碳酸镁.写出该反应的化学方程式MgCO3+2HCl═MgCl2+H2O+CO2↑.
(2)乙和丙二位同学运用如图提供的装置,分别设计实验方案,进一步确认该胃药的主要成分.虚线方框中的装置从如图B、C中选择组装.(装置气密性良好,装置中空气的影响忽略不计)
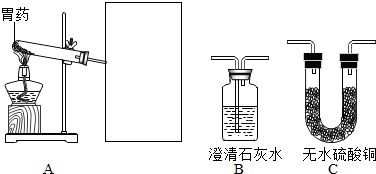
【交流反思】实验小组经过交流与反思,认为乙同学的实验过程中存在一处错误,请你指出该错误并说明理由:B、C装置连接顺序错误;气体先通过B装置会带出水蒸气,干扰水的检验.
【查阅资料】①MgCO3受热能分解,且MgCO3的化学性质与CaCO3相似;
②Al(OH)3受热分解生成Al2O3和H2O;③药品中的其它成分不参与反应.
【实验探究】
(1)甲同学取少量该胃药于试管中,加入适量稀盐酸,观察到有气泡产生.说明该胃药中含有MgCO3或碳酸镁.写出该反应的化学方程式MgCO3+2HCl═MgCl2+H2O+CO2↑.
(2)乙和丙二位同学运用如图提供的装置,分别设计实验方案,进一步确认该胃药的主要成分.虚线方框中的装置从如图B、C中选择组装.(装置气密性良好,装置中空气的影响忽略不计)

| 实验过程 | 实验现象 | 实验结论 |
| 乙同学选用B、C装置,按A→B→C顺序连接,点燃酒精灯加热 | B中澄清石灰水变浑浊, C中无水硫酸铜变为蓝色. | 该胃药中含有MgCO3、Al(OH)3 |
| 丙同学也选用B、C装置,按A→C→B顺序连接,点燃酒精灯加热 | C中无明显现象,B中澄清石灰水变浑浊. | 该胃药中不含有Al(OH)3或氢氧化铝 |
5.拒绝铺张浪费,提倡低碳健康的生活理念已渐入人心.下列行为不符合这一理念的是( )
| A. | 开发新能源,如利用太阳能热水器等 | |
| B. | 尽量使用一次性筷子和餐具以防传染病 | |
| C. | 在外就餐时,把没吃完的剩菜打包带走 | |
| D. | 多步行和骑人力自行车,减少自驾汽车 |
2.观察是学习化学的一种方法.下列有关实验现象描述正确的是( )
| A. | 铜丝在空气中灼烧一段时间,铜丝加热变蓝 | |
| B. | 铁丝在氧气中剧烈燃烧、火星四射、生成白色固体 | |
| C. | 分别点燃一小块棉纤维和羊毛纤维,都产生了烧焦羽毛的气味 | |
| D. | 将一块生石灰投入到装有适量水的烧杯中,一段时间后烧杯外壁发烫 |
7.已知氢氧化钾(KOH)可溶于水,其化学性质与氢氧化钠相似.下列各组物质能够共存的是( )
| A. | 氢氧化钾溶液与稀硫酸 | B. | 氢氧化钾溶液与稀盐酸 | ||
| C. | 氢氧化钾溶液与氯化钡溶液 | D. | 氢氧化钾溶液与硫酸铜溶液 |
 SO2是一种无色有刺激性气味的有毒气体,密度比空气大,易溶于水,排放到空气中会形成酸雨.实验室用如图装置收集一瓶干燥的SO2,装置的导管
SO2是一种无色有刺激性气味的有毒气体,密度比空气大,易溶于水,排放到空气中会形成酸雨.实验室用如图装置收集一瓶干燥的SO2,装置的导管