题目内容
味精是常用的调味品,某味精由谷氨酸钠(化学式为C5H8NO4Na)和少量的氯化钠组成,为了测定该味精中谷氨酸钠的含量,进行如下实验:取该味精样品5.50 g,溶于蒸馏水中,加入足量的硝酸银溶液,反应的化学方程式为:NaCl+AgNO3=AgCl↓+NaNO3(谷氨酸钠与硝酸银溶液不反应).充分反应后过滤、洗涤、烘干、称量,得到沉淀1.35 g.计算:
(1)该味精中谷氨酸钠的质量分数(计算结果精确的1%)
(2)实用该味精3.60 g,能为人体提供多少可钠元素?(计算结果精确的0.01 g)
答案:
解析:
解析:
|
则该味精中谷氨酸钠的质量分数为:(5.50 g-0.546 g)/5.50 g×100%=90% (2)3.6 g味精样品中含有谷氨酸钠的质量为:3.6 g×90%=3.24 g 则食用3.6 g味精含钠元素质量为:3.24 g×23/169×100%+(3.6 g-3.24 g)×23/58.5×100%=0.58 g |

练习册系列答案
相关题目
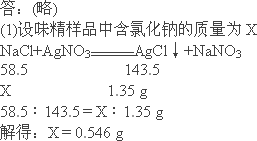
 味精是常用的调味品,它的鲜味来自于其中的主要成分“谷氨酸钠”(化学式是C5H8NO4Na).某品牌味精包装上标注内容如图所示,请回答:
味精是常用的调味品,它的鲜味来自于其中的主要成分“谷氨酸钠”(化学式是C5H8NO4Na).某品牌味精包装上标注内容如图所示,请回答: