题目内容
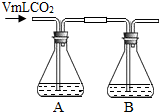 某同学用如下实验装置探究CO2与NaOH溶液能否反应.锥形瓶中的溶液为氢氧化钠溶液或澄清石灰水(均为200mL).
某同学用如下实验装置探究CO2与NaOH溶液能否反应.锥形瓶中的溶液为氢氧化钠溶液或澄清石灰水(均为200mL).【查阅资料】通常状况下,1体积水能溶解1体积二氧化碳
①A中的溶液是
②请判断V
③如果不用B装置,实验后向锥形瓶A中的溶液中加入
考点:碱的化学性质
专题:常见的碱 碱的通性
分析:根据氢氧化钠溶液与二氧化碳反应生成碳酸钠和水,二氧化碳与氢氧化钙溶液反应生成碳酸钙白色沉淀和水,生成的碳酸钠能与稀盐酸反应生成二氧化碳气体,能与澄清的石灰水反应生成碳酸钙白色沉淀,据此结合题意进行分析解答.
解答:解:①氢氧化钠溶液与二氧化碳反应生成碳酸钠和水,二氧化碳与氢氧化钙溶液反应生成碳酸钙白色沉淀和水,将二氧化碳先通入氢氧化钠溶液中,二氧化碳被氢氧化钠溶液吸收,再通入澄清石灰水中无明显变化,说明氢氧化钠溶液可以与二氧化碳反应.
②氢氧化钠溶液与二氧化碳反应,由题意,通常状况下,1体积水能溶解1体积二氧化碳,故通入的二氧化碳气体的体积应大于200mL.
③氢氧化钠与稀盐酸反应生成氯化钠和水,碳酸钠能与稀盐酸反应生成二氧化碳气体,能与澄清的石灰水反应生成碳酸钙白色沉淀,如果不用B装置,实验后向锥形瓶A中的溶液中加入稀盐酸(或氢氧化钙溶液),若产生气泡(或沉淀),说明二氧化碳和氢氧化钠溶液反应.
故答案为:①氢氧化钠溶液;澄清石灰水;石灰水没有变浑浊;②>;③稀盐酸 ( 或氢氧化钙溶液);气泡(或沉淀).
②氢氧化钠溶液与二氧化碳反应,由题意,通常状况下,1体积水能溶解1体积二氧化碳,故通入的二氧化碳气体的体积应大于200mL.
③氢氧化钠与稀盐酸反应生成氯化钠和水,碳酸钠能与稀盐酸反应生成二氧化碳气体,能与澄清的石灰水反应生成碳酸钙白色沉淀,如果不用B装置,实验后向锥形瓶A中的溶液中加入稀盐酸(或氢氧化钙溶液),若产生气泡(或沉淀),说明二氧化碳和氢氧化钠溶液反应.
故答案为:①氢氧化钠溶液;澄清石灰水;石灰水没有变浑浊;②>;③稀盐酸 ( 或氢氧化钙溶液);气泡(或沉淀).
点评:本题难度不大,熟练掌握碱的化学性质、碳酸钠的检验方法并能灵活运用是正确解答本题的关键.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
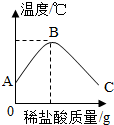 盐酸滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化如图所示,下列叙述错误的是( )
盐酸滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化如图所示,下列叙述错误的是( )| A、从A到B过程中,烧杯中溶液的pH逐渐减小 |
| B、稀盐酸与氢氧化钠溶液发生的反应是放热反应 |
| C、B点表示酸碱恰好完全反应 |
| D、随稀盐酸的加入,反应放出的热量由少变多,再由多变少 |
氨气(NH3)燃烧反应的化学方程式为4NH3+3O2
6H2O+2N2.该反应属于( )
| ||
| A、置换反应 | B、化合反应 |
| C、分解反应 | D、复分解反应 |
关于“物质-在氧气中燃烧的主要现象--所属反应类型”的描述中正确的是( )
| A、碳--发出白光--化合反应 |
| B、硫--微弱淡蓝火焰--氧化反应 |
| C、铁--火星四射--分解反应 |
| D、蜡烛-发出白光,有水雾--氧化反应 |