题目内容
7.含杂质的Fe2O3固体样品20g,高温下用足量的CO完全还原(杂质不与CO反应),将生成的CO2气体用足量的澄清石灰水充分吸收后,产生30g白色沉淀.则下列说法正确的是( )
| A. | 通入的CO质量为8.4g | B. | 还原后的固体质量为11.2g | ||
| C. | 样品中氧化铁的质量分数为80% | D. | 样品中氧元素质量分数一定为24% |
分析 根据一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,依据碳酸钙沉淀的质量进行计算.
解答 解:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,CO2+Ca(OH)2=CaCO3↓+H2O,所以
Fe2O3---3CO---2Fe----3CaCO3↓,
160 84 112 300
16g 8.4g 11.2g 30g
A、理论上需要通入一氧化碳的质量为8.4g,但是在反应前后都需要通入一氧化碳,所以实际通入的CO质量大于8.4g,故A错误;
B、还原后铁的质量为11.2g,固体质量包括杂质质量,大于11.2g,故B错误;
C、样品中氧化铁的质量分数为:$\frac{16g}{20g}$×100%=80%,故C正确;
D、杂质中是否含有氧元素,不能确定,所以样品中氧元素质量分数可能为:$\frac{\frac{48}{160}×16g}{20g}$×100%=24%,故D错误.
故选:C.
点评 本题主要考查了一氧化碳还原氧化铁的实验,难度不大,需要结合实际的实验操作进行计算.

练习册系列答案
相关题目
17.下列属于纯净物的是( )
| A. | 液态氮 | B. | 加碘盐 | C. | 食用醋 | D. | 冰红茶 |
15.工业生产中利用焦炭和水无原料制取水煤气(主要成分是CO和H2),发生的化学变化用化学方程式表示为C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2,下列说法错误的是( )
| A. | 该化学变化属于置换反应 | |
| B. | 变化过程中表现氧化性的物质是水 | |
| C. | 变化过程中一定不会造成空气污染 | |
| D. | 变化过程得到的水煤气可以作为燃料使用 |
2.化学实验是进行科学探究的重要方式,具备基本的化学实验技能是学习化学和进行探究活动的基础.下列实验操作正确的是( )
| A. | 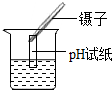 测溶液pH | B. | 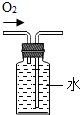 排水法收集氧气 | C. | 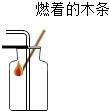 CO2气体验满 | D. |  给液体加热 |
12.下列说法正确的是( )
| A. | 煤气泄漏,用明火查看 | B. | 金属回收,可节能防污 | ||
| C. | 油锅着火,可加水浇灭 | D. | 明矾净水,能杀菌消毒 |
19.如图实验或说法不合理的是( )
| A. |  实验中黄铜片能在铜片上刻画出痕迹,说明黄铜的硬度比铜片小 | |
| B. |  实验中烧杯C中浓氨水会变红 | |
| C. |  实验中镁在CO2中剧烈燃烧,说明燃烧不一定需要氧气 | |
| D. |  实验既能说明CO能与氧化铁反应,也能说明CO具有可燃性 |
16.Fe2O3、ZnO、CuO的固体混合粉末6.42克,在加热条件下用足量CO还原,得到金属混合物4.82克,将生成的
CO2气体用足量的澄清石灰水吸收后,产生X克白色沉淀,则X的数值为( )
CO2气体用足量的澄清石灰水吸收后,产生X克白色沉淀,则X的数值为( )
| A. | 12 | B. | 11 | C. | 10 | D. | 9 |
17.下列图象能正确反映对应的变化关系的是( )
| A. |  加热一定量的高锰酸钾固体 | |
| B. |  向盛有一定量碳酸钙粉末的烧杯中加入稀盐酸 | |
| C. |  用等质量、等浓度的过氧化氢溶液制氧气 | |
| D. |  向等质量的镁、铁两种金属,分别放入同浓度的稀硫酸 |