题目内容
18.炭雕(见图1)是一种集观赏与空气净化为一体的产品.这种产品可对车内及室内空气中的一氧化碳、甲醛等有害气体进行有效吸附.某课外小组想对炭雕产品进行初步探究.[提出问题]炭雕产品中是否含有碳元素.

[猜想与假设]炭雕产品中含有碳元素
[查阅资料]①碳在空气中完全燃烧只生成二氧化碳,不完全燃烧
生成二氧化碳和一氧化碳.②新鲜的人或动物血液,遇一氧化碳由鲜红变为暗红.
[设计实验]通过检验炭雕产品燃烧产物,证明炭雕产品中含有碳元素.组装所需仪器如图2.
(1)A装置的作用为吸收空气中的水和二氧化碳,其中氧化钙与水反应的化学方程式为CaO+H2O=Ca(OH)2.
(2)实验开始后,C装置中有白色沉淀,C装置发生化学反应方程式为Ca(OH)2+CO2=CaCO3↓+H2O,E装置中新鲜的鸡血变为暗红色,则证明CO气体.
(3)写出B、C装置中的仪器名称.
①铁架台②硬质玻璃管③酒精灯④试管.
分析 A装置除去了空气中的水蒸汽和二氧化碳,B装置氧气与炭雕粉末在加热条件下发生反应,C装置检验反应的生成物中是否有二氧化碳,D装置除去反应生成的二氧化碳,E装置检验反应的生成物中是否有一氧化碳.
解答 3解:(1)氧化钙与水反应生成氢氧化钙,化学方程式为CaO+H2O=Ca(OH)2
(2)澄清的石灰水变浑浊说明石灰水中通入了二氧化碳.故选Ca(OH)2+CO2=CaCO3↓+H2O.
因为新鲜的人或动物血液,遇一氧化碳由鲜红变为暗红,而本题中的实验现象是新鲜的鸡血变为暗红色,故答案为:炭雕产品燃烧产物中有一氧化碳产生.
(3)B、C装置中的仪器名称分别是铁架台、硬质玻璃管、酒精灯、试管.
故答案为:(1)CaO+H2O=Ca(OH)2
(2)Ca(OH)2+CO2=CaCO3↓+H2O;CO;
(3)铁架台、硬质玻璃管、酒精灯、试管.
点评 检验一氧化碳最安全的方法是通入新鲜血液,若加热或点燃,都有可能发生爆炸的危险.

练习册系列答案
相关题目
9.某校化学小组同学从家里带来食盐、水垢、纯碱、淀粉和洗衣粉5种物质.老师从中取出3种物质,研磨混合均匀(如图所示),让同学们检验其成分.他们在查阅资料后,用5种已知物的性质实验作参照,探究未知粉末的成分.
(1)小组同学用5种已知物做性质实验.
每次取样方法如图所示:
5种已知物的实验记录:
根据上述实验记录回答:
①该洗衣粉溶液pH>7(填“>”、“<”或“=”);
②写出纯碱与稀盐酸反应的化学方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑.
(2)小组同学用未知粉末重复上述实验进行成分探究.
未知粉末的实验记录:
参照5种已知物的性质实验,分析未知粉末的成分:
未知粉末中一定含有的两种物质是淀粉和洗衣粉,还含有的第三种物质是水垢或纯碱,请你设计检验第三种物质的实验方案取未知粉末于试管中,加入足量的水充分溶解、过滤.向滤液中加入稀盐酸,若有大量的气泡产生,则第三种物质是纯碱;若无大量的气泡产生,则第三种物质是水垢.
(1)小组同学用5种已知物做性质实验.
每次取样方法如图所示:

5种已知物的实验记录:
| 实验过程 | 部分实验现象 |
| 实验1:加水溶解 取样,分别加入足量的水充分溶解 | 淀粉、水垢:均有白色浑浊,试管底部有不溶物 洗衣粉:溶解,有洗涤剂泡沫浮于液面 |
| 实验2:加酚酞溶液 向实验1所得液体中分别滴入2滴无色酚酞溶液 | 洗衣粉、纯碱:液体呈红色 其余物质:均无明显变化 |
| 实验3:加稀盐酸 另取样品,分别加入2mL稀盐酸 | 洗衣粉:有洗涤剂泡沫浮于液面 水垢:有大量气体逸出 食盐、淀粉:均无气体产生 |
| 实验4:加碘水 另取样品,分别滴入2滴碘水 | 淀粉:变蓝其余物质:均不变蓝 |
①该洗衣粉溶液pH>7(填“>”、“<”或“=”);
②写出纯碱与稀盐酸反应的化学方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑.
(2)小组同学用未知粉末重复上述实验进行成分探究.
未知粉末的实验记录:
| 实验1 加水溶解 | 实验2 加酚酞溶液 | 实验3 加稀盐酸 | 实验4 加碘水 | |
| 未知粉末实验现象 | 白色浑浊,试管底部有不溶物,有洗涤剂泡沫浮于液面 | 液体呈红色 | 有大量气体逸出 | 变蓝 |
未知粉末中一定含有的两种物质是淀粉和洗衣粉,还含有的第三种物质是水垢或纯碱,请你设计检验第三种物质的实验方案取未知粉末于试管中,加入足量的水充分溶解、过滤.向滤液中加入稀盐酸,若有大量的气泡产生,则第三种物质是纯碱;若无大量的气泡产生,则第三种物质是水垢.
13.在水、二氧化碳、二氧化硫、氧气的组成中都含有( )
| A. | 氧元素 | B. | 氧气分子 | C. | 氧气 | D. | 以上各项都有 |
3.常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.
(1)试管尾部放一团湿棉花的目的是提供水蒸气.
(2)探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中.说明生成的气体是H2.
(3)探究试管中剩余固体成分是什么?
【查阅资料】
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引.
【猜想与假设】猜想一:剩余固体是Fe与Fe3O4;
猜想二:剩余固体是Fe3O4.
【实验探究】
【实验结论】铁和水蒸气反应的化学方程式为3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2.
【反思与交流】该黑色固体不可能是Fe2O3,理由是Fe2O3红棕色粉末且不能被磁铁吸引.
(1)试管尾部放一团湿棉花的目的是提供水蒸气.
(2)探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中.说明生成的气体是H2.
(3)探究试管中剩余固体成分是什么?
【查阅资料】
| 常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 能否被磁铁吸引 | 否 | 否 | 能 |
【猜想与假设】猜想一:剩余固体是Fe与Fe3O4;
猜想二:剩余固体是Fe3O4.
【实验探究】
| 实验操作 | 实验现象及结论 |
| 取少量黑色固体于试管中,加入足量的稀盐酸 | 若固体全部溶解,没有气泡冒出,剩余固体是Fe3O4;若固体全部溶解,有气泡冒出,剩余固体是Fe与Fe3O4 |
【反思与交流】该黑色固体不可能是Fe2O3,理由是Fe2O3红棕色粉末且不能被磁铁吸引.
10.保护环境、保护空气清洁的有效措施是( )
| A. | 大力植树绿化 | B. | 用石油代替煤 | ||
| C. | 减少城市人口 | D. | 加强工业排气管理? |
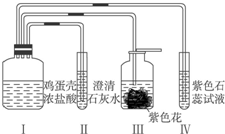 某同学做“证明鸡蛋壳的主要成分是碳酸盐”的实验时,设计了如下方案,经检验装置气密性合格后加入试剂.
某同学做“证明鸡蛋壳的主要成分是碳酸盐”的实验时,设计了如下方案,经检验装置气密性合格后加入试剂.