题目内容
13.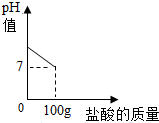 在含氯化钠杂质的纯碱样品12.4g中逐渐加入质量分数为7.3%稀盐酸,所加稀盐酸的质量与溶液的pH值的关系如图所示,计算:
在含氯化钠杂质的纯碱样品12.4g中逐渐加入质量分数为7.3%稀盐酸,所加稀盐酸的质量与溶液的pH值的关系如图所示,计算:(1)100g稀盐酸中氯化氢的质量7.3g.
(2)纯碱样品中,纯碱的质量.
(3)恰好完全反应时,所得溶液中溶质的质量分数?
分析 碳酸钠与稀盐酸反应生成氯化钠、水和二氧化碳;由所加稀盐酸的质量关系图,滴加至100g时,前后完全反应,据此由稀盐酸的质量、溶质的质量分数由反应的化学方程式计算出生成氯化钠的质量、参加反应的碳酸钠的质量、生成二氧化碳气体的质量,进而计算出所得溶液中溶质的质量分数即可.
解答 解:(1)100g稀盐酸中氯化氢的质量为100g×7.3%=7.3g.
(2)设反应中碳酸钠、氯化钠、二氧化碳的质量分别为x、y、z,
Na2CO3+2HCl=2NaCl+CO2↑+H2O
106 73 117 44
x 7.3g y z
$\frac{106}{x}=\frac{73}{7.3g}=\frac{117}{y}=\frac{44}{z}$
x=10.6g
y=11.7g
z=4.4g
所得溶液的质量分数为$\frac{11.7g+12.4g-10.6g}{12.4g+100g-4.4g}$×100%≈12.5%.
答:(1)7.3g;(2)纯碱样品中,纯碱的质量为10.6g;(3)所得溶液的质量分数为12.5%.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,细致地分析图示信息,找出完全反应时消耗的稀盐酸的质量是正确解答本题的前提和关键.

练习册系列答案
相关题目
16.下列关于溶液的说法正确的是( )
| A. | 均一、稳定的液体一定是溶液 | |
| B. | 用汽油洗去衣服上的油污是乳化现象 | |
| C. | 碘酒中的溶剂是酒精 | |
| D. | 无色、透明的液体一定是溶液 |
8.某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
【假设猜想】针对疑问,太家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是四.
理由氢氧化钠和硫酸会发生反应
【实验探究】(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有氢氧化钠.
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaCl2溶液、Na2CO3溶液,进行如下三个方案的探究.
【得出结论】通过探究,全班同学一致确定猜想二是正确的.
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出
【实验探究】
(2)中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:①实验操作中的错误是pH试纸浸入溶液中.
②实验方案中也有一个是错误的,错误的原因是Na2SO4与BaCl2反应也会生成白色沉淀,不能证明一定有H2SO4存在.
③请你再设计一个方案验证猜想(要求写出步骤、现象、结论)并写出相应方程式.
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
【假设猜想】针对疑问,太家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是四.
理由氢氧化钠和硫酸会发生反应
【实验探究】(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有氢氧化钠.
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaCl2溶液、Na2CO3溶液,进行如下三个方案的探究.
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 |  |  |  |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出
【实验探究】
(2)中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:①实验操作中的错误是pH试纸浸入溶液中.
②实验方案中也有一个是错误的,错误的原因是Na2SO4与BaCl2反应也会生成白色沉淀,不能证明一定有H2SO4存在.
③请你再设计一个方案验证猜想(要求写出步骤、现象、结论)并写出相应方程式.
18.物质都是由微粒构成的.下列物质由分子构成的是( )
| A. | 二氧化碳 | B. | 氯化钠 | C. | 金刚石 | D. | 铜 |
5.维生素C(C6H8O6)主要存在于蔬菜和水果中,它能促进人体生长发育,增强人体对疾病的抵抗力.近年来,科学家还发现维生素 C 有防癌作用.下列关于维生素 C 的说法中错误的是( )
| A. | 维生素 C 是氧化物 | |
| B. | 维生素 C 是由6个碳元素、8个氢元素、6个氧元素组成 | |
| C. | 维生素 C 中,C、H、O三种元素的质量比为 9:1:12 | |
| D. | 青少年应多吃蔬菜水果,切忌偏食 |
2.酸碱指示剂紫色石蕊变色情况( )
| A. | 遇酸溶液变红色,遇碱溶液也变红色 | |
| B. | 遇酸溶液变蓝色,遇碱溶液也变蓝色 | |
| C. | 遇酸溶液变红色,遇碱溶液变蓝色 | |
| D. | 遇酸溶液变蓝色,遇碱溶液变红色 |
3.张大爷去年购买的化肥外包装上的字迹看不清,只记得是K2CO3、NH4Cl、KCl中的一种.小明利用学过的化学知识,设计如下实验方案帮张大爷鉴别化肥.
【实验步骤】取少量上述化肥于一容器中,加入少量Ca(OH)2粉末,混合研磨.
【实验现象】未嗅到刺激性的氨味.
【实验结论】小明由上述实验推断该化肥不是NH4Cl.
(1)请根据上述实验结论,设计一个简单的实验方案来进一步证明该化肥可能是什么.
【实验步骤】取少量上述化肥于一容器中,加入少量Ca(OH)2粉末,混合研磨.
【实验现象】未嗅到刺激性的氨味.
【实验结论】小明由上述实验推断该化肥不是NH4Cl.
(1)请根据上述实验结论,设计一个简单的实验方案来进一步证明该化肥可能是什么.
| 实验步骤 | 实验现象 | 结论或有关化学反应方程式 |
| 取样,溶解,滴加少量稀盐酸 | 产生气泡 | 该化肥是K2CO3 方程式:K2CO3+2HCl═2KCl+H2O+CO2↑ |
 人类的生产生活离不开金属材料,随着科技水平的不断提高,金属及其合金在日常生活中扮演着越来越重要的角色.
人类的生产生活离不开金属材料,随着科技水平的不断提高,金属及其合金在日常生活中扮演着越来越重要的角色.