题目内容
据报道,某市一运输电石的汽车因未做好防水工作,在运输途中突降小雨,引发车厢内着火.已知电石(主要成分是碳化钙,化学式为CaC2)本身不可燃,与水反应后生成一种无色具有可燃性的气体乙炔(化学式C2H2).
(1)电石与水反应属于 反应(填“吸热”或“放热”);
(2)碳化钙中碳元素的化合价为 ;
(3)电石与水反应的化学方程式为:CaC2+2H2O=X+C2H2↑,则X的化学式为 ;
(4)根据上述信息,你认为电石应 保存.
(1)电石与水反应属于
(2)碳化钙中碳元素的化合价为
(3)电石与水反应的化学方程式为:CaC2+2H2O=X+C2H2↑,则X的化学式为
(4)根据上述信息,你认为电石应
考点:物质发生化学变化时的能量变化,有关元素化合价的计算,质量守恒定律及其应用
专题:结合课本知识的信息
分析:(1)燃烧的条件:可燃物、温度达着火点、与氧气接触;由题意“电石(CaC2)不可燃,与水接触剧烈反应产生乙炔(C2H2)”,既然燃烧,温度肯定达着火点;所以反应放出热量;
(2)根据化合价原则由化学式求出元素的化合价.
(3)根据质量守恒定律反应前后原子的种类、数目不变,推测X的化学式;
(4)根据电石的性质分析保存的方法.
(2)根据化合价原则由化学式求出元素的化合价.
(3)根据质量守恒定律反应前后原子的种类、数目不变,推测X的化学式;
(4)根据电石的性质分析保存的方法.
解答:解:(1)燃烧的条件:可燃物、温度达着火点、与氧气接触;由题意“电石(CaC2)不可燃,与水接触剧烈反应产生乙炔(C2H2)”,既然燃烧,温度肯定达着火点;所以反应放出热量;
(2)在CaC2种由钙元素显+2价,可求出碳元素的化合价为-1价;
(3)根据质量守恒定律和化学方程式可知,X中含有Ca的个数为1,含有C的个数为2-2=0,含有H的个数为2×2-2=2,含有O的个数为2;则X的化学式为:Ca(OH)2;
(4)由于电石能与水反应,电石应密封防水保存.
故答为:(1)放热;(2)-1;(3)Ca(OH)2;(4)密封防水.
(2)在CaC2种由钙元素显+2价,可求出碳元素的化合价为-1价;
(3)根据质量守恒定律和化学方程式可知,X中含有Ca的个数为1,含有C的个数为2-2=0,含有H的个数为2×2-2=2,含有O的个数为2;则X的化学式为:Ca(OH)2;
(4)由于电石能与水反应,电石应密封防水保存.
故答为:(1)放热;(2)-1;(3)Ca(OH)2;(4)密封防水.
点评:本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目
 去年10月,石墨烯的制备者获得了诺贝尔奖.石墨烯是从石墨材料中剥离出来的单层固体单质(结构如图),它不仅是已知材料中最薄的一种,还非常牢固坚硬.关于石墨烯的说法中错误的是( )
去年10月,石墨烯的制备者获得了诺贝尔奖.石墨烯是从石墨材料中剥离出来的单层固体单质(结构如图),它不仅是已知材料中最薄的一种,还非常牢固坚硬.关于石墨烯的说法中错误的是( )| A、石墨烯与C60是同一种物质 |
| B、石墨烯是一种单质 |
| C、石墨烯的硬度很大 |
| D、石墨烯完全燃烧后的产物是CO2 |
石头纸是一种新型、环保纸张.它与传统的木浆纸不同,是将碳酸钙粉末加上15%的聚乙烯和5%的胶合剂,经特殊工艺处理后制成.下列说法正确的是( )
| A、聚乙烯是一种天然有机高分子材料 |
| B、石头纸的应用有利于节能减排 |
| C、利用稀盐酸可以区别石头纸与木浆纸 |
| D、石头纸极易溶于水便于回收再利用 |
类推是化学学习中常用的一种重要思维方法.下列类推结果中正确的是( )
| A、原子由核外电子、质子和中子构成,所以原子核中一定含有质子和中子 |
| B、H2点燃前需验纯,所以可燃性气体点燃前都需验纯 |
| C、酸与碱的中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 |
| D、有机物都含碳元素,所以含碳元素的化合物一定都是有机物 |
甲烷在一定量的氧气中燃烧,测得反应前后各物质的质量如表所示:下列判断正确的是( )
| 物质 | 甲烷 | 氧气 | 水 | 二氧化碳 | X |
| 反应前质量/g | 3.2 | 11.2 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 7.2 | 4.4 | a |
| A、表中a的值为2.6 |
| B、X一定是该反应的催化剂 |
| C、X可能含有氢元素 |
| D、若增加氧气量,则生成物的种类可能减少 |


 如图是实验室所用硫酸试剂瓶上标签的部分内容,请仔细阅读后计算:
如图是实验室所用硫酸试剂瓶上标签的部分内容,请仔细阅读后计算: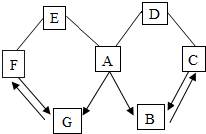 如图所示 A~G 是初中化学常见的物质.图中“→”表示转化关系,“-”表示相互能反应.已知 B 是光合作用的原料,G 是最清洁的能源,且 B、C、D、E、F 都是氧化物.请回答:
如图所示 A~G 是初中化学常见的物质.图中“→”表示转化关系,“-”表示相互能反应.已知 B 是光合作用的原料,G 是最清洁的能源,且 B、C、D、E、F 都是氧化物.请回答: